0 129549 129557 129563 129567 129573 129575 129579 129585 129587 129593 129599 129603 129605 129609 129615 129617 129623 129627 129629 129633 129635 129639 129641 129643 129644 129645 129647 129648 129649 129651 129653 129657 129659 129663 129665 129669 129675 129677 129683 129687 129689 129693 129699 129705 129707 129713 129717 129719 129725 129729 129735 129743 203614


 利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 下面给出了四种烃A、B、C、D的相关信息:
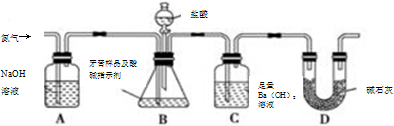
下面给出了四种烃A、B、C、D的相关信息: 为测定氨分子中氮、氢原子个数比,某研究性学习小组用浓氨水和氧化钙反应制取氨气,然后用氨气与氧化铜粉末发生氧化还原反应.设计了如下实验流程:实验中,先检查装置气密性;然后用制得的氨气排尽洗气瓶前所有装置中的空气;再连接洗气瓶和气体测量装置;立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
为测定氨分子中氮、氢原子个数比,某研究性学习小组用浓氨水和氧化钙反应制取氨气,然后用氨气与氧化铜粉末发生氧化还原反应.设计了如下实验流程:实验中,先检查装置气密性;然后用制得的氨气排尽洗气瓶前所有装置中的空气;再连接洗气瓶和气体测量装置;立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.