题目内容
某溶液可能含CO3-、SO4-、HCO3-中的一种或两种离子.小明取出两份相同的上述样品溶液于两个试管中,向其中一份加入过量盐酸,产生无色气体;向另一份滴加过量氯化钡溶液,产生白色沉淀.
请设计方案,在小明实验的基础上对溶液进行探究.
可供选择的仪器用品和试剂:烧杯、试管、玻璃棒、胶头滴管、漏斗、滤纸、铁架台;盐酸;稀硝酸;氯化钡溶液、酚酞试剂、蒸馏水.
(1)提出溶液中三种离子CO3-、SO4-、HCO3-存在的假设:
假设1:只存在CO32-
假设2:存在CO32-和SO42-
假设3: ;
假设4:存在SO42-和HCO3-
(2)基于假设1:①CO32-水解的离子方程式为 .
②若要验证CO32-已水解,则可向溶液滴入 ,观察溶液颜色的变化.
(3)基于假设2,请设计方案,将实验操作、预期的现象和结论填入下表
请设计方案,在小明实验的基础上对溶液进行探究.
可供选择的仪器用品和试剂:烧杯、试管、玻璃棒、胶头滴管、漏斗、滤纸、铁架台;盐酸;稀硝酸;氯化钡溶液、酚酞试剂、蒸馏水.
(1)提出溶液中三种离子CO3-、SO4-、HCO3-存在的假设:
假设1:只存在CO32-
假设2:存在CO32-和SO42-
假设3:
假设4:存在SO42-和HCO3-
(2)基于假设1:①CO32-水解的离子方程式为
②若要验证CO32-已水解,则可向溶液滴入
(3)基于假设2,请设计方案,将实验操作、预期的现象和结论填入下表
| 步骤编号 | 实验操作 | 预期现象和结论 |
| 1. | 取少量溶液于试管中,滴入 | |
| 2. | 往装有沉淀的试管中加入 |
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:(1)向一份样品溶液中加入过量的盐酸,产生无色气泡,说明溶液中含有CO32-和HCO3-的一种或两种;向另一份样品溶液中滴加过量的氯化钡溶液,产生白色沉淀,说明溶液中可能有CO32-和SO42-中的一种或两种;
(2)基于假设1:①CO32-水解的离子方程式为:CO32-+H2O=
+OH-;
②若要验证CO32-已水解,则可向溶液滴入酚酞,酚酞遇碱变红色;
(3)欲证明溶液中只有CO32-和SO42-,先向溶液中加入过量的氯化钡溶液过滤,然后向生成的白色沉淀中滴加过量的盐酸,分析结论即可.
(2)基于假设1:①CO32-水解的离子方程式为:CO32-+H2O=
| HCO | - 3 |
②若要验证CO32-已水解,则可向溶液滴入酚酞,酚酞遇碱变红色;
(3)欲证明溶液中只有CO32-和SO42-,先向溶液中加入过量的氯化钡溶液过滤,然后向生成的白色沉淀中滴加过量的盐酸,分析结论即可.
解答:
解:(1)向一份样品溶液中加入过量的盐酸,产生无色气泡,说明溶液中含有CO32-和HCO3-的一种或两种;向另一份样品溶液中滴加过量的氯化钡溶液,产生白色沉淀,说明溶液中可能有CO32-和SO42-中的一种或两种.故溶液中离子的存在有四种可能性:①溶液中只存在CO32-;②溶液中存在CO32-和SO42--;③溶液中存在CO32-和HCO3;④溶液中存在HCO3-和SO42-,
故答案为:假设3:溶液中存在CO32-和HCO3-;
(2)基于假设1:①CO32-水解的离子方程式为:CO32-+H2O=HCO3-+OH-;
故答案为:CO32-+H2O=HCO3-+OH-;
②若要验证CO32-已水解,则可向溶液滴入酚酞,酚酞遇碱变红色;故答案为:酚酞;
(3)欲证明溶液中只有CO32-和SO42-,可先向溶液中加入过量的氯化钡溶液过滤,然后向生成的白色沉淀中滴加过量的盐酸,观察沉淀是否溶解,沉淀部分溶解,说明原溶液中一定含有SO42-、CO32-;
故答案为:过量的氯化钡溶液;产生白色沉淀;过量的盐酸;沉淀部分溶解.
故答案为:假设3:溶液中存在CO32-和HCO3-;
(2)基于假设1:①CO32-水解的离子方程式为:CO32-+H2O=HCO3-+OH-;
故答案为:CO32-+H2O=HCO3-+OH-;
②若要验证CO32-已水解,则可向溶液滴入酚酞,酚酞遇碱变红色;故答案为:酚酞;
(3)欲证明溶液中只有CO32-和SO42-,可先向溶液中加入过量的氯化钡溶液过滤,然后向生成的白色沉淀中滴加过量的盐酸,观察沉淀是否溶解,沉淀部分溶解,说明原溶液中一定含有SO42-、CO32-;
故答案为:过量的氯化钡溶液;产生白色沉淀;过量的盐酸;沉淀部分溶解.
点评:本题考查物质的检验及鉴别,明确物质的性质是解答本题的关键,注意物质性质的差异即可解答,题目难度不大.

练习册系列答案
相关题目
铅蓄电池在现代生活中有广泛的应用.其电极材料是Pb和PbO2,电解质是稀硫酸.Pb+PbO2+2H2SO4
2PbSO4+2H2O,下列说法正确的是( )
| 放电 |
| 充电 |
| A、铅蓄电池使用一段时间后要添加硫酸 |
| B、电池充电时,阴极反应为:Pb-2e-+SO42-═PbSO4 |
| C、电池充电时,电池正极应和电源的正极相连接 |
| D、电池放电时,电池正极周围溶液pH不断增大 |
下列叙述正确的是( )
| A、白铁(镀锌)的表面一量破损,铁腐蚀加快 |
| B、原电池中电子向负极流动 |
| C、马口铁(镀锡)的表面一旦破损,铁腐蚀加快 |
| D、用铝质铆钉接铁板,铁易被腐蚀 |
 导致空气污染的主要原因来自于化石燃料燃烧、硫酸工业和汽车尾气的排放;致使大量二氧化硫和氮氧化物排入大气中.利用化学反应原理研究治理环境污染的方法是当前环保工作的重要研究内容之一.
导致空气污染的主要原因来自于化石燃料燃烧、硫酸工业和汽车尾气的排放;致使大量二氧化硫和氮氧化物排入大气中.利用化学反应原理研究治理环境污染的方法是当前环保工作的重要研究内容之一.

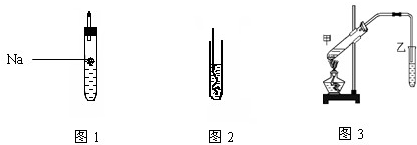
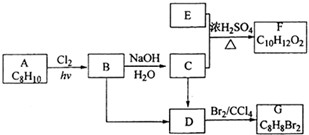
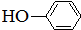 合成
合成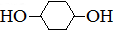 .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)