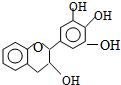
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图.关于EGC的下列叙述中正确的是( )| A、分子中所有的原子共面 |
| B、1mol EGC能与4mol NaOH反应 |
| C、可以发生氧化反应、取代反应、加成反应、消去反应 |
| D、能与FeCl3溶液发生显色反应 |
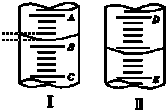 如图,图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,图Ⅱ表示50mL滴定管中液面的位置,D与E刻度间相差1mL.如果刻度A和D都是4,则两处液面的读数是( )
如图,图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,图Ⅱ表示50mL滴定管中液面的位置,D与E刻度间相差1mL.如果刻度A和D都是4,则两处液面的读数是( )| A、Ⅰ中是3.2mL,Ⅱ中是3.40mL |
| B、Ⅰ中是4.8mL,Ⅱ中是3.40mL |
| C、Ⅰ中是3.2mL,Ⅱ中是4.60mL |
| D、Ⅰ中是4.8mL,Ⅱ中是4.60mL |
下列有机物的名称中不正确的是?( )
| A、3-乙基戊烷 |
| B、2,3-二甲基戊烷? |
| C、2,2-二甲基-2-乙炔 |
| D、2-甲基-4-乙基庚烷 |
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
| A、加热 |
| B、稀硫酸改用98%的浓硫酸 |
| C、滴加少量CuSO4溶液 |
| D、铁片改用铁粉 |
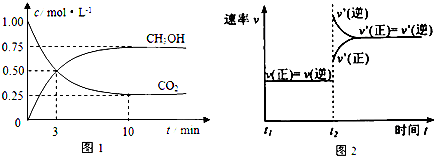
在一定温度下,将等物质的量的CO和水蒸气通入恒容密闭容器中,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),一段时间后达到平衡.对该平衡状态描述正确的是( )
| A、CO2浓度不变 |
| B、正反应速率大于逆反应速率 |
| C、正反应速率等于逆反应速率 |
| D、正反应速率小于逆反应速率 |
下列化学实验现象描述正确的是( )
| A、湿润的红色石蕊试纸遇二氧化硫变蓝色 |
| B、酚酞试液滴入稀硫酸溶液中显红色 |
| C、氯气使干燥的红布条褪色 |
| D、葡萄糖溶液中滴加新制氢氧化铜溶液出现砖红色色沉淀 |
正确的存放化学药品,是化学实验基本要求之一.下列物质存放错误的是( )
| A、漂白粉长期敞口放置于广口瓶中 |
| B、金属钠存放于煤油中 |
| C、水玻璃盛放在带橡皮塞的试剂瓶中 |
| D、浓硝酸存放在棕色试剂瓶中 |