题目内容
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0 (填“>”“<”或“=”);
(2)能判断该反应达到化学平衡状态的依据是 (多选扣分).
(a)容器中压强不变 (b)混合气体中c(CO)不变(c)v正(H2)=v逆(H2O)(d)c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9?c(CO2)?c(H2)=c(CO)?c(H2O),试判断此时的温度为 ℃.其它条件不变,升高温度,原化学平衡向 反应方向移动(填“正”或“逆”).
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡.若反应开始时CO与H2O的浓度分别为0.200mol?L-1和0.100mol?L-1,平衡时CO的转化率为 .
其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的平衡常数表达式K=
(2)能判断该反应达到化学平衡状态的依据是
(a)容器中压强不变 (b)混合气体中c(CO)不变(c)v正(H2)=v逆(H2O)(d)c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9?c(CO2)?c(H2)=c(CO)?c(H2O),试判断此时的温度为
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡.若反应开始时CO与H2O的浓度分别为0.200mol?L-1和0.100mol?L-1,平衡时CO的转化率为
考点:化学平衡的计算,化学平衡状态的判断
专题:
分析:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;由表中数据可知,温度越高化学平衡常数越大,升高温度平衡向正反应移动,正反应是吸热反应;
(2)化学平衡状态的标志:正逆反应速率相等;
(3)计算平衡常数的值,可找出对应温度;
(4)根据三段式计算出平衡时各组分的物质的量,从而计算平衡时CO的转化率.
(2)化学平衡状态的标志:正逆反应速率相等;
(3)计算平衡常数的值,可找出对应温度;
(4)根据三段式计算出平衡时各组分的物质的量,从而计算平衡时CO的转化率.
解答:
解:(1)可逆反应CO2(g)+H2(g)?CO(g)+H2O(g)的化学平衡常数表达式k=
,由表中数据可知,温度越高化学平衡常数越大,升高温度平衡向正反应移动,正反应是吸热反应,故答案为:
;>;
(2)a、反应是一个反应前后体积不变的反应,压强的改变不会要引起平衡移动,故a错误;
b、化学平衡时,各组分的浓度不随时间的改变而改变,故b正确;
c、化学平衡状态的标志是v正=v逆,所以v正(H2)=v正(H2O)表明反应达到平衡状态,故c正确;
d、c(CO2)=c(CO)时,取决起始浓度和转化率,不能判断达到了平衡状态,故d错误.
故答案为:bc.
(3)由0.9?c(CO2)?c(H2)=c(CO)?c(H2O),可知k=
=0.9,对应温度为800℃,其它条件不变,升高温度,原化学平衡向吸热方向移动,故向正反应方向移动,故答案为:800;正;
(4)CO(g)+H2O(g)?CO2(g)+H2(g)
开始(mol?L-1):0.200 0.100 0 0
变化(mol?L-1):x x x x
平衡(mol?L-1):0.200-x 0.100-x x x
K=
=
=1.0,解得x=
,
故平衡后CO的转化率为
=
,
故答案为:
.
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| c(CO)c(H2O) |
| c(CO2)c(H2) |
(2)a、反应是一个反应前后体积不变的反应,压强的改变不会要引起平衡移动,故a错误;
b、化学平衡时,各组分的浓度不随时间的改变而改变,故b正确;
c、化学平衡状态的标志是v正=v逆,所以v正(H2)=v正(H2O)表明反应达到平衡状态,故c正确;
d、c(CO2)=c(CO)时,取决起始浓度和转化率,不能判断达到了平衡状态,故d错误.
故答案为:bc.
(3)由0.9?c(CO2)?c(H2)=c(CO)?c(H2O),可知k=
| c(CO)c(H2O) |
| c(CO2)c(H2) |
(4)CO(g)+H2O(g)?CO2(g)+H2(g)
开始(mol?L-1):0.200 0.100 0 0
变化(mol?L-1):x x x x
平衡(mol?L-1):0.200-x 0.100-x x x
K=
| c(CO2)c(H2) |
| c(CO)c(H2O) |
| x×x |
| (0.200-x)×(0.100-x) |
| 2 |
| 30 |
故平衡后CO的转化率为
| ||
| 0.200 |
| 1 |
| 3 |
故答案为:
| 1 |
| 3 |
点评:本题考查化学平衡状态的判断,化学平衡常数的计算等知识,难度中等,注意平衡常数只与温度有关.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目
下列各离子浓度的大小比较,正确的是( )
| A、同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl④NH3?H2O,C(NH4+)由大到小的顺序是:①>③>②>④ |
| B、常温时,将等体积的盐酸和氨水混合后,pH=7,则C(NH4+)>C (Cl-) |
| C、0.2 mol/LNa2CO3溶液中:C (OH-)=C (HCO3-)+C (H+)+C (H2CO3) |
| D、同浓度的下列溶液中,①NaCl ②Na2CO3 ③CH3COONa④NaOH,pH值由大到小的顺序是:④>③>②>① |
下列每组中各有三种混合物,它们都能用分液漏斗分离的是( )
| A、乙酸乙酯和水,酒精和水,植物油和水 |
| B、甘油和水,乙酸和水,乙酸和乙醇 |
| C、四氯化碳和水,溴苯和水,硝基苯和水 |
| D、汽油和水,苯和水,乙醛和水 |
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
| A、加热 |
| B、稀硫酸改用98%的浓硫酸 |
| C、滴加少量CuSO4溶液 |
| D、铁片改用铁粉 |
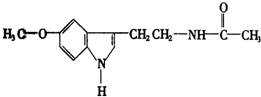 “今年过节不收礼,收礼还收脑白金”,反应了中国人收礼的习俗,脑白金中有效成分的结构简式如图,下列对该化合物的叙述正确的是( )
“今年过节不收礼,收礼还收脑白金”,反应了中国人收礼的习俗,脑白金中有效成分的结构简式如图,下列对该化合物的叙述正确的是( )| A、它属于芳香烃,含有碳碳双键和肽键,能使高锰酸钾溶液和溴水褪色,但原理不同 |
| B、它属于高分子化合物,所有原子不可能共面 |
| C、分子式C13N2H16O2,能和盐酸发生化学反应,体现了一定的碱性 |
| D、在一定条件下可以发生加成反应、氧化反应、水解反应,不能发生酯化反应 |
下列关于
He的说法正确的是( )
3 2 |
| A、与 42He互为同位素 |
| B、中子数为3 |
| C、带2个单位正电荷 |
| D、原子最外层有1个电子 |
