X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如图所示.X的最高价氧化物和气态氢化物的分子都是由极性键形成的非极性分子.下列性质比较中正确的是( )
| X | Y | |||
| Z | W |
| A、最高价氧化物的水化物的酸性:Y<X<W |
| B、离子半径由小到大的顺序:W<Z<Y |
| C、单质晶体的熔点由低到高的顺序:Y<W<Z |
| D、原子最外层的电子数:Z<Y<X |
下列有关活化能的说法正确的是( )
| A、Ag+和Cl-在水溶液中混合,其反应的活化能接近于零 |
| B、活化能的大小对化学反应前后的能量变化能产生影响 |
| C、加催化剂能降低正反应的活化能,但不降低逆反应的活化能 |
| D、温度降低,反应速率减慢,其原因是降低了反应的活化能 |
对于反应H2(g)+Cl2(g)═2HCl(g)(该反应为放热反应)的能量变化描述正确的是( )
| A、反应物总能量小于成物总能量 |
| B、断键和成键过程中都释放能量 |
| C、断键过程中吸收能量,成键过程中释放能量 |
| D、断键过程中释放能量,成键过程中吸收能量 |
化学反应中一定伴随着能量的变化,下列有关能量的说法错误的是( )
| A、水的电离是吸热过程 |
| B、任何中和反应都是放热反应 |
| C、电解饱和食盐水时,电能转变成化学能 |
| D、由2H2(g)+O2(g)?2H2O(g)△H=-483.6kj?mol-1,可知的燃烧热为241.8kJ?mol-1 |
一定量的稀硫酸与过量的锌反应,为减慢反应速率,且不影响生成氢气的总量,可向稀硫酸中加入适量的下列物质,其中一定不能达到目的是( )
| A、氯化钠溶液 | B、水 |
| C、醋酸钾溶液 | D、硫酸铜固体 |
对于硫酸工业中SO2的催化氧化反应:2SO2+O2
2SO3,下列说法错误的是( )
| 催化剂 |
| 加热 |
| A、使用催化剂是为了加快反应速率 |
| B、增大O2浓度可以使SO2转化率达到100% |
| C、加压可以增大反应速率 |
| D、增大O2浓度可以增大反应速率 |
2-丁炔与1,3-丁二烯分别跟氢气反应的热化学方程式如下:
CH3-C≡C-CH3(g)+2H2(g)→CH3CH2CH2CH3(g)+Q1
CH2=CH-CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g)+Q2
已知:Q1>Q2(Q1和Q2均大于零),由此不能判断( )
CH3-C≡C-CH3(g)+2H2(g)→CH3CH2CH2CH3(g)+Q1
CH2=CH-CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g)+Q2
已知:Q1>Q2(Q1和Q2均大于零),由此不能判断( )
| A、2-丁炔与1,3-丁二烯稳定性的相对大小 |
| B、2-丁炔与1,3-丁二烯分子储存能量的相对高低 |
| C、2-丁炔与1,3-丁二烯相互转化的热效应 |
| D、一个碳碳叁键的键能与两个碳碳双键的键能之和的大小 |
下列实验事实不能用勒沙特列原理解释的是( )
A、 | ||||||
B、 | ||||||
C、 | ||||||
D、
|
能将化学能转化为电能的装置(烧杯中溶液均为稀硫酸)是( )
A、 |
B、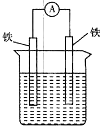 |
C、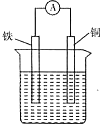 |
D、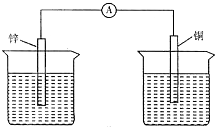 |
有科学家提出硅是“21世纪的能源”、“未来的石油”的观点.假如硅作为一种普遍使用的新型能源被开发利用,下列关于其有利因素的说法中,你认为不妥的是( )
| A、便于运输、储存,从安全角度考虑,硅是最佳的燃料 |
| B、自然界的含硅化合物易开采 |
| C、硅燃烧放出的热量大,燃烧产物对环境污染程度低且容易有效控制 |
| D、自然界中存在大量单质硅 |