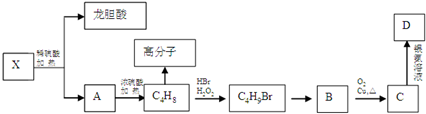
下列对聚丙烯的描述错误的是( )
| A、聚丙烯的分子长链是由C-C键连接而成的 |
| B、聚丙烯的分子长链上有支链 |
| C、聚丙烯每个链节主链上有2个碳原子 |
| D、聚丙烯能使溴水褪色 |
下列叙述错误的是( )
| A、加热能杀死流感病毒是因为病毒的蛋白质受热变性 |
| B、人造纤维、含成纤维和光导纤维都是有机高分子化合物 |
| C、在汽车排气管上加装“催化转化器”怒为了减少有害气体的排放 |
| D、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
下列物质的保存方法不正确的是( )
| A、氢氟酸在塑料瓶中保存 |
| B、盛液溴的试剂瓶常加少量水 |
| C、少量的金属钠应保存在煤油中 |
| D、固态碘放在棕色细口瓶中 |
用已经准确称量过的NaOH固体配制500mL1mol/L的NaOH溶液,供选择的仪器有:①玻璃棒②分液漏斗③胶头滴管④容量瓶⑤烧杯⑥烧瓶,必须选用的仪器有( )
| A、②③④ | B、①③④⑤ |
| C、③④⑤⑥ | D、①②④ |
下列物质中可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是( )
| A、钠 | B、溴水 |
| C、碳酸钠溶液 | D、氢氧化钠溶液 |
鉴别Cl-、Br-、I-三种离子,不宜选用的试剂组是( )
| A、AgNO3溶液和稀硝酸 |
| B、溴水和淀粉溶液 |
| C、氯水和CCl4溶液 |
| D、氯水和淀粉溶液 |
通过实验可验证蔗糖水解可以生成葡萄糖,实验包括下列操作:其操作的正确顺序是( )
①加入少量蔗糖和水制成溶液 ②水浴加热 ③加入NaOH溶液中和酸并至溶液呈碱性 ④加入新制备的Cu(OH)2 ⑤加入少量稀硫酸 ⑥再加热.
①加入少量蔗糖和水制成溶液 ②水浴加热 ③加入NaOH溶液中和酸并至溶液呈碱性 ④加入新制备的Cu(OH)2 ⑤加入少量稀硫酸 ⑥再加热.
| A、①②⑤⑥④③ |
| B、①⑤②④⑥③ |
| C、①⑤②③④⑥ |
| D、①⑥④⑤③② |
只用一种试剂就可将AgNO3、KSCN、稀H2SO4、NaOH四种无色溶液区分开,该试剂是( )
| A、BaCl2溶液 |
| B、FeCl2溶液 |
| C、FeCl3溶液 |
| D、Fe(NO3)3溶液 |
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.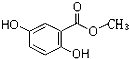 .
.