铜片和锌片用导线连接后,插入稀硫酸中,锌片是( )
| A、正极 |
| B、负极 |
| C、电子流入的一极 |
| D、发生还原反应的一极 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl.下列“水”电池在海水中放电时的有关说法正确的是( )
| A、正极反应式:Ag+Cl--e-═AgCl |
| B、每生成2 molNa2Mn5O10转移1 mol电子 |
| C、AgCl是还原产物 |
| D、Na+不断向“水”电池的正极移动 |
下列关于化学平衡常数的说法正确的是( )
| A、化学平衡发生移动,平衡常数必发生变化 |
| B、平衡常数发生变化,化学平衡必发生移动 |
| C、改变浓度,平衡常数一定改变 |
| D、催化剂改变达到平衡的时间,必引起平衡常数的改变 |
一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )


| A、反应的化学方程式为:2M?N |
| B、0~t1时间段内,平均反应速率v(N)﹕v(M)=2﹕1 |
| C、t2时,正逆反应速率相等,达到平衡 |
| D、t3时,正反应速率大于逆反应速率 |
化学在环境保护中有着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染,其降解NO3-的原理如图所示.下列说法错误的是( )

| A、A为电源正极,e-移动方向:B→Ag/Pt电极→Pt电极→A |
| B、铂电极为阳极,电极反应为4OH--4e-=2H2O+O2↑ |
| C、Ag/Pt电极为阴极,电极反应为2NO3-+6H2O+10e-=N2↑+12OH- |
| D、若电解过程中转移了4mol电子,则膜两侧电解液的质量变化差为28克 |
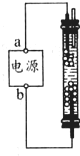 某学生想制作一种家作环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收制得有较强杀菌能力的消毒液,设计了如图所示的装置,以下对电源电极名称和消毒液的主要成份判断正确的是( )
某学生想制作一种家作环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收制得有较强杀菌能力的消毒液,设计了如图所示的装置,以下对电源电极名称和消毒液的主要成份判断正确的是( )| A、a为正极,b为负极;NaClO和NaCl |
| B、a为负极,b为正极;NaClO和NaCl |
| C、a为阳极,b为阴极;NaClO和NaCl |
| D、a为阳极,b为阴极;NaClO和NaCl |
用惰性电极电解下列溶液一段时间后,再加入一定质量的另一物质(中括号内),溶液能与原来溶液完全一样的是( )
①CuCl2[Cu]②AgNO3[Ag2O]③NaCl[HCl]④CuSO4[Cu(OH)2].
①CuCl2[Cu]②AgNO3[Ag2O]③NaCl[HCl]④CuSO4[Cu(OH)2].
| A、①② | B、②③ | C、①④ | D、③④ |
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.(1)NO2可用水吸收,相应的化学反应方程式为
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.(1)NO2可用水吸收,相应的化学反应方程式为