题目内容
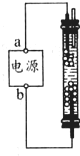 某学生想制作一种家作环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收制得有较强杀菌能力的消毒液,设计了如图所示的装置,以下对电源电极名称和消毒液的主要成份判断正确的是( )
某学生想制作一种家作环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收制得有较强杀菌能力的消毒液,设计了如图所示的装置,以下对电源电极名称和消毒液的主要成份判断正确的是( )| A、a为正极,b为负极;NaClO和NaCl |
| B、a为负极,b为正极;NaClO和NaCl |
| C、a为阳极,b为阴极;NaClO和NaCl |
| D、a为阳极,b为阴极;NaClO和NaCl |
考点:电解原理
专题:
分析:电解池中,阳极是阴离子放电,阴极是阳离子放电,氯气能和氢氧化钠反应生成次氯酸钠,可以制得有较强杀菌能力的消毒液.
解答:
解:电解氯化钠溶液时,阳极是氯离子失电子生成氯气的过程,阴极是氢离子的电子生成氢气的过程,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,所以一定要让氯气在下边电极产生,所以下边的电极是阳极,上边的电极是阴极,即a为负极,b为正极,氯气和氢氧化钠反应生成的是氯化钠和次氯酸钠.
故选B.
故选B.
点评:本题是一道电解原理和实际相结合的题目,要熟记电解池的工作原理,学以致用.

练习册系列答案
相关题目
关于化学键的下列叙述中,正确的是( )
| A、所有物质中都含有化学键 |
| B、共价化合物中可能含离子键 |
| C、离子化合物中只含离子键 |
| D、离子化合物中可能含共价键 |
无机化学命名委员会在1989年作出决定,把长式元素周期表原先的主、副族及族号取消,由左到右改为18列.按此规定,下列说法中错误的是( )
| A、第15列元素的最高价氧化物的化学式是R2O3 |
| B、第1列和第17列元素单质熔、沸点变化趋势相反 |
| C、第11列中肯定没有非金属元素 |
| D、在18列元素中,第3列的元素种类最多 |
观察图示装置,下列说法错误的是( )


| A、虚线框中接灵敏电流计,该装置可将化学能转化为电能 | ||||
B、虚线框中接直流电源,可能发生:Cu+H2SO4
| ||||
C、虚线框中接直流电源,可能发生:Zn+H2SO4
| ||||
| D、生成2.24L H2时,一定转移0.2 mol e- |
把a、b、c、d四块金属浸泡在稀硫酸中,用导线两两相连可以组成各种原电池:若a、b相连时,a为负极;c、d相连时,c为负极;a、c相连时,c为正极;b、d相连时,b为正极,则这四种金属的活泼性由强到弱为( )
| A、a b c d |
| B、a c d b |
| C、c a b d |
| D、b d c a |
理论上不能设计为原电池的化学反应是( )
A、CH4(g)+2O2 (g)
| ||||
| B、HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(aq)△H<0 | ||||
C、2H2 (g)+O2(g)
| ||||
| D、2FeCl3(aq)+Fe(s)═3FeCl2 (aq)△H<0 |
甲乙两容器中均充入2mol SO2、1mol O2,发生反应2SO2(g)+O2(g)?2SO3(g)+Q,已知甲为恒温恒压容器,乙为恒温恒容容器.初始时两容器的温度体积相同.一段时间后反应达到平衡,为使两容器中的SO2在平衡混合物的物质的量分数相同,下列措施中可行的是( )
| A、向甲容器中充入一定量的氦气 |
| B、向甲容器中充入一定量的SO3气体 |
| C、升高乙容器的温度 |
| D、增大甲容器的压强 |
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.(1)NO2可用水吸收,相应的化学反应方程式为
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.(1)NO2可用水吸收,相应的化学反应方程式为 (1)按官能团的不同可以对有机物进行分类,请指出下列有机物的种类,填在横线上.
(1)按官能团的不同可以对有机物进行分类,请指出下列有机物的种类,填在横线上.