 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42-向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu→Zn
⑥正极反应式:Cu+2e-═Cu2+,发生氧化反应.
| A、①②③ | B、②④⑥ |
| C、③④⑤ | D、②④ |
25℃、101kPa条件下,反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ?mol -1能自发进行的原因( )
| A、是吸热反应 |
| B、是放热反应 |
| C、是熵减小的反应 |
| D、是熵增效应大于热效应 |
在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( ) 

| A、碳棒上有气体放出,溶液pH变大 |
| B、a是负极,b是正极 |
| C、导线中有电子流动,电流从a极到b极 |
| D、a极上发生了氧化反应 |
据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染,其电池反应为2Zn+O2═2ZnO,原料为锌粒、电解液和空气,则下列叙述正确的是( )
①锌为正极,空气进入负极反应
②负极反应为Zn+2OH-→ZnO+H2O+2e-
③正极发生氧化反应
④电解液肯定不是强酸.
①锌为正极,空气进入负极反应
②负极反应为Zn+2OH-→ZnO+H2O+2e-
③正极发生氧化反应
④电解液肯定不是强酸.
| A、①② | B、①③ | C、②③ | D、②④ |
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A、最简单气态氢化物的热稳定性:R>Q |
| B、最高价氧化物对应水化物的酸性:Q<W |
| C、原子半径:T>Q>R |
| D、R的最高价氧化物对应的水化物和它的氢化物反应不能生成盐 |
下列各组反应中,不属于可逆反应的是( )
A、N2+3H2
| ||||||||
B、H2+I2
| ||||||||
C、2H2+O2
| ||||||||
D、2SO2+O2
|
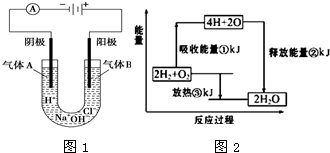 (1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化.已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收 249kJ的能量;形成水分子中1mol H-O键能够释放 463kJ能量.如图1表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上.
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化.已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收 249kJ的能量;形成水分子中1mol H-O键能够释放 463kJ能量.如图1表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上. 对如图中两极加以必要的连接并填空:
对如图中两极加以必要的连接并填空: 现有如下两个反应:(A)NaOH+HCl═NaCl+H2O (B)2FeCl3+Cu═2FeCl2+CuCl2
现有如下两个反应:(A)NaOH+HCl═NaCl+H2O (B)2FeCl3+Cu═2FeCl2+CuCl2