题目内容
 现有如下两个反应:(A)NaOH+HCl═NaCl+H2O (B)2FeCl3+Cu═2FeCl2+CuCl2
现有如下两个反应:(A)NaOH+HCl═NaCl+H2O (B)2FeCl3+Cu═2FeCl2+CuCl2(1)根据两反应本质,判断
(2)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料、电解质溶液及电极反应式电极反应式:负极:
(3)铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:铅蓄电池的负极材料是
考点:原电池和电解池的工作原理,设计原电池
专题:
分析:(1)能自发进行的放热的氧化还原反应能设计成原电池;
(2)失电子发生氧化反应的金属作负极,不如负极活泼的金属或导电的非金属作正极,得电子的电解质溶液作电解质溶液;
(3)根据电池反应式知,Pb元素化合价由0价、+4价变为+2价,得电子化合价降低的反应物为正极、失电子化合价升高的金属为负极;
放电时,H2SO4参加反应导致溶液中c( H+)降低;放电时,电解质溶液中阳离子向正极移动、阴离子向负极移动.
(2)失电子发生氧化反应的金属作负极,不如负极活泼的金属或导电的非金属作正极,得电子的电解质溶液作电解质溶液;
(3)根据电池反应式知,Pb元素化合价由0价、+4价变为+2价,得电子化合价降低的反应物为正极、失电子化合价升高的金属为负极;
放电时,H2SO4参加反应导致溶液中c( H+)降低;放电时,电解质溶液中阳离子向正极移动、阴离子向负极移动.
解答:
解:(1)(A)NaOH+HCl=NaCl+H2O不是氧化还原反应,所以不能设计成原电池,(B)2FeCl3+Cu═2FeCl2+CuCl2是自发进行的放热的氧化还原反应,所以能设计成原电池,故答案为:B;
(2)在2FeCl3+Cu═2FeCl2+CuCl2反应中,FeCl3被还原,为正极反应,可用碳棒作正极,电极反应为2Fe3++2e-=2Fe2+,Cu被氧化,为原电池负极反应,电极反应为Cu-2e-=Cu2+,该反应中FeCl3得电子发生还原反应,所以电解质溶液是FeCl3溶液,
故答案为:Cu-2e-=Cu2+;2Fe3++2e-=2Fe2+; ;
;
(3)根据电池反应式知,Pb元素化合价由0价、+4价变为+2价,失电子化合价升高的金属为负极,则Pb为负极;
放电时,H2SO4参加反应导致溶液中c( H+)降低,则溶液pH增大,酸性减小,放电时,电解质溶液中阳离子向正极移动、阴离子向负极移动,
故答案为:Pb;减小;负.
(2)在2FeCl3+Cu═2FeCl2+CuCl2反应中,FeCl3被还原,为正极反应,可用碳棒作正极,电极反应为2Fe3++2e-=2Fe2+,Cu被氧化,为原电池负极反应,电极反应为Cu-2e-=Cu2+,该反应中FeCl3得电子发生还原反应,所以电解质溶液是FeCl3溶液,
故答案为:Cu-2e-=Cu2+;2Fe3++2e-=2Fe2+;
 ;
;(3)根据电池反应式知,Pb元素化合价由0价、+4价变为+2价,失电子化合价升高的金属为负极,则Pb为负极;
放电时,H2SO4参加反应导致溶液中c( H+)降低,则溶液pH增大,酸性减小,放电时,电解质溶液中阳离子向正极移动、阴离子向负极移动,
故答案为:Pb;减小;负.
点评:本题考查原电池的设计及其铅蓄电池的反应原理,本题难度不大,注意原电池的组成特点和反应原理,注意电极反应式的书写,为常考查知识.

练习册系列答案
相关题目
能与银氨溶液发生银镜反应,且其水解产物也能发生银镜反应的糖类是( )
| A、葡萄糖 | B、麦芽糖 |
| C、乙酸乙酯 | D、淀粉 |
 某有机物的结构如图所示,下列选项中均不正确的是( )
某有机物的结构如图所示,下列选项中均不正确的是( )①可以燃烧;②能跟Na反应;③分子式为C11H10O2;④能发生酯化反应;⑤能发生加聚反应;⑥能发生水解反应;⑦含有4种官能团.
| A、①③④ | B、②⑤⑥ |
| C、③⑥⑦ | D、④⑥⑦ |
下列装置能形成原电池且灵敏电流计发生偏转的是( )
A、 氯化铁溶液 |
B、 稀硫酸 |
C、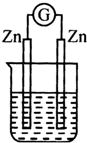 硫酸铜溶液 |
D、 乙醇 |
 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42-向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu→Zn
⑥正极反应式:Cu+2e-═Cu2+,发生氧化反应.
| A、①②③ | B、②④⑥ |
| C、③④⑤ | D、②④ |
下列说法正确的( )
| A、放热反应在常温下一定容易进行 |
| B、植物的光合作用是把太阳能转化为热能的过程 |
| C、反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的 |
| D、凡是在加热或点燃条件下进行的反应都是吸热反应 |
根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
部分短周期元素的原子半径及主要化合价
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
| A、氢氧化物碱性:G<L<M |
| B、非金属性:T<Q |
| C、气态氢化物的稳定性:R<T |
| D、L2+与T2-的核外电子数相等 |
已知A为ⅡA族元素,B为ⅢA族元素,它们的原子序数分别为m和n,且A、B为同一周期的元素,下列关系式错误的是( )
| A、n=m+1 |
| B、n=m+11 |
| C、n=m+25 |
| D、n=m+18 |