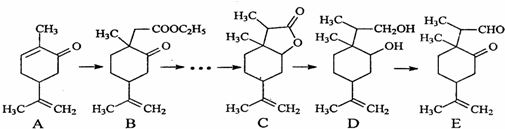
某厂对三价铝回收与再利用工艺如下,(硫酸浸出液中金属离子主要是Cr3+,其次是Fe2+,Fe3+,Al3+,Ca2+

常温下,部分阳离子以氢氧化物形式沉淀时溶液的PH见下表:
下列叙述不正确的是:( )

常温下,部分阳离子以氢氧化物形式沉淀时溶液的PH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr2+ |
| 开始沉淀时的PH | 1.9 | 7.0 | 9.6 | - | - |
| 沉淀完全时的PH | 3.2 | 9.0 | 11.1 | 8 | 9(>9)溶解 |
| A、加入H2O2的作用只是将Fe2+氧化为Fe3+ |
| B、调节溶液的pH=8是为了除去Fe3+和Al3+ |
| C、还原过程发生的反应为:2Na2Cr2O7+3SO2+12H2O=2Cr(OH)(H2O)5SO4+Na2SO4 |
| D、钠离子交换树脂的原理为:Mn++nNaR=MRn+nNa+,被交换除去的杂质离子是Ca2+和Mg2+ |
用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列操作会导致测定结果偏低的是( )
| A、读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
| B、滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C、酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D、酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
下列实验操作,对实验结果不会产生影响的是( )
| A、用酸碱中和滴定法测定未知浓度的碱液时,在锥形瓶中加人2-3 mL酚酞试液作指示剂 |
| B、用蒸馏水湿润pH试纸后测定硫酸钠溶液的pH |
| C、测定中和反应的反应热时,将碱溶液缓慢倒入酸溶液中 |
| D、在淀粉溶液中加入稀硫酸加热一段时间后,向其中滴加银氨溶液检验淀粉的水解产物 |


 酸碱中和滴定是中学化学常见实验.
酸碱中和滴定是中学化学常见实验.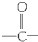 )的化合物
)的化合物 (R,R′代表烷基或H原子)发生缩合反应生成新的有机物和水,苯酚还可跟酰氯
(R,R′代表烷基或H原子)发生缩合反应生成新的有机物和水,苯酚还可跟酰氯 反应生成有机酸酯,例如
反应生成有机酸酯,例如