0 110252 110260 110266 110270 110276 110278 110282 110288 110290 110296 110302 110306 110308 110312 110318 110320 110326 110330 110332 110336 110338 110342 110344 110346 110347 110348 110350 110351 110352 110354 110356 110360 110362 110366 110368 110372 110378 110380 110386 110390 110392 110396 110402 110408 110410 110416 110420 110422 110428 110432 110438 110446 203614
 2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )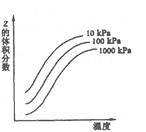
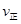 增大,
增大,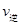 减小,平衡向右移动
减小,平衡向右移动 Fe(SCN)3+3KCl中加入KCl固体,平衡将向逆反应方向移动,溶液颜色将变浅
Fe(SCN)3+3KCl中加入KCl固体,平衡将向逆反应方向移动,溶液颜色将变浅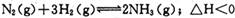 达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示。下列有关叙述一定正确的是
达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示。下列有关叙述一定正确的是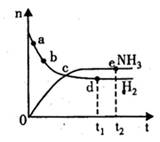
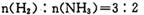
 2HI(g);△H<0,有相同容积的密封容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入0.1mol H2和0.2molI2,相同温度下分别达到平衡。下列说法不正确的是
2HI(g);△H<0,有相同容积的密封容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入0.1mol H2和0.2molI2,相同温度下分别达到平衡。下列说法不正确的是 2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。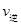 (X2)=2
(X2)=2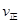 (Y2) d.容器内的密度保持不变
(Y2) d.容器内的密度保持不变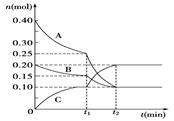
 N2O4(g) ,平衡后,向容器内再充入1mol N2O4(g),下列说法正确的( )
N2O4(g) ,平衡后,向容器内再充入1mol N2O4(g),下列说法正确的( )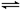 Ag2O(s)+SO3(g),2SO3(g)
Ag2O(s)+SO3(g),2SO3(g)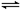 CO2(g)+NO(g),(正反应放热),达到平衡后,只改变其中一个条件,对平衡的影响是:
CO2(g)+NO(g),(正反应放热),达到平衡后,只改变其中一个条件,对平衡的影响是:
 3A(g)+B(g)
3A(g)+B(g)  2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白:
2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白: