0 110067 110075 110081 110085 110091 110093 110097 110103 110105 110111 110117 110121 110123 110127 110133 110135 110141 110145 110147 110151 110153 110157 110159 110161 110162 110163 110165 110166 110167 110169 110171 110175 110177 110181 110183 110187 110193 110195 110201 110205 110207 110211 110217 110223 110225 110231 110235 110237 110243 110247 110253 110261 203614
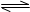 2C(g)+D(g),达到平衡时C的浓度为wmol/L保持温度和压强不变,按下列四种配比充入容器P中,平衡后C的浓度仍为wmol/L的是( )
2C(g)+D(g),达到平衡时C的浓度为wmol/L保持温度和压强不变,按下列四种配比充入容器P中,平衡后C的浓度仍为wmol/L的是( ) 2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的
2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的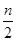 )
)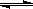 N2O4,下列状态一定是平衡状态的是
N2O4,下列状态一定是平衡状态的是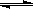 3 C(g)达到平衡时,测得c(A)=0.5 mol/L。在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)=0.20mol/L。下列判断中正确的是
3 C(g)达到平衡时,测得c(A)=0.5 mol/L。在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)=0.20mol/L。下列判断中正确的是 eC(气)+fD(气),反应过程中保持其他条件不变,C的体积分
eC(气)+fD(气),反应过程中保持其他条件不变,C的体积分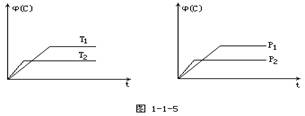
 CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的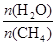 恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示: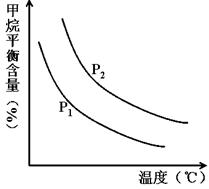
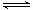 pC(g)+qD(g) △H<0。下列结论中错误的是
pC(g)+qD(g) △H<0。下列结论中错误的是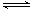 2SO3(g) △H=-198kJ·mol-1
2SO3(g) △H=-198kJ·mol-1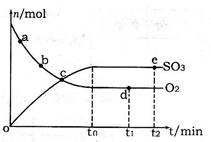
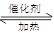 2SO3 △H<0。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述正确的是
2SO3 △H<0。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述正确的是