0 109121 109129 109135 109139 109145 109147 109151 109157 109159 109165 109171 109175 109177 109181 109187 109189 109195 109199 109201 109205 109207 109211 109213 109215 109216 109217 109219 109220 109221 109223 109225 109229 109231 109235 109237 109241 109247 109249 109255 109259 109261 109265 109271 109277 109279 109285 109289 109291 109297 109301 109307 109315 203614






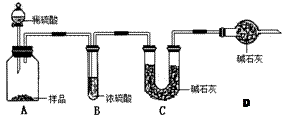
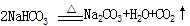 。请回答:
。请回答: 成 功
成 功 成 功
成 功