0 106491 106499 106505 106509 106515 106517 106521 106527 106529 106535 106541 106545 106547 106551 106557 106559 106565 106569 106571 106575 106577 106581 106583 106585 106586 106587 106589 106590 106591 106593 106595 106599 106601 106605 106607 106611 106617 106619 106625 106629 106631 106635 106641 106647 106649 106655 106659 106661 106667 106671 106677 106685 203614

 )="2.0" mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
)="2.0" mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )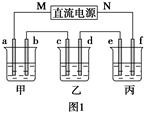

 R2Cu(有机相)+2H+(水相)
R2Cu(有机相)+2H+(水相)