0 106490 106498 106504 106508 106514 106516 106520 106526 106528 106534 106540 106544 106546 106550 106556 106558 106564 106568 106570 106574 106576 106580 106582 106584 106585 106586 106588 106589 106590 106592 106594 106598 106600 106604 106606 106610 106616 106618 106624 106628 106630 106634 106640 106646 106648 106654 106658 106660 106666 106670 106676 106684 203614

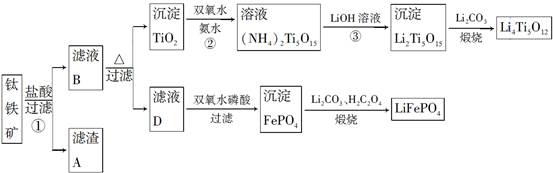
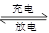 Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。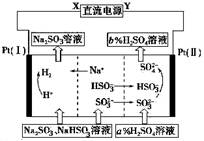
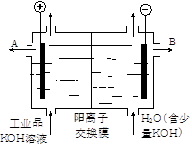
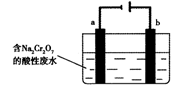
 KIO3 + 3H2↑。下列说法中正确的是
KIO3 + 3H2↑。下列说法中正确的是 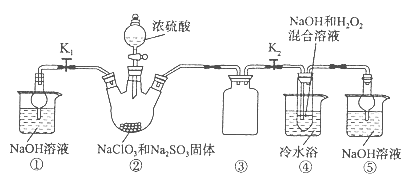
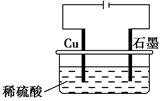
 CuSO4+H2↑
CuSO4+H2↑