题目内容
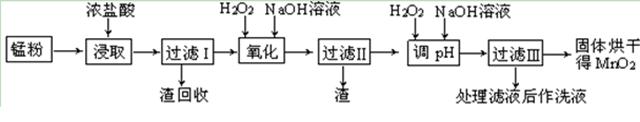
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如图所示:
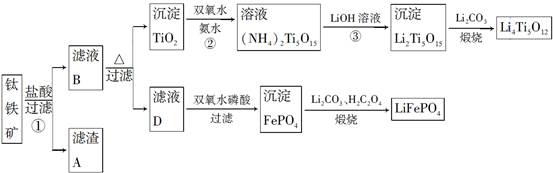
已知:FeTiO3与盐酸反应的离子方程式为FeTiO3+4H++4Cl-=Fe2++TiOCl42—+2H2O
(1)化合物FeTiO3中铁元素的化合价是________。
(2)滤渣A的成分是________。
(3)滤液B中TiOCl42—转化生成TiO2的离子方程式是________________。
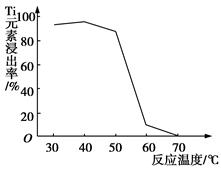
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti元素浸出率下降的原因是________________________________。
(5)反应③的化学方程式是________________________。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是________。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)做电极组成电池,其工作原理为Li4Ti5O12+3LiFePO4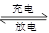 Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。

已知:FeTiO3与盐酸反应的离子方程式为FeTiO3+4H++4Cl-=Fe2++TiOCl42—+2H2O
(1)化合物FeTiO3中铁元素的化合价是________。
(2)滤渣A的成分是________。
(3)滤液B中TiOCl42—转化生成TiO2的离子方程式是________________。
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti元素浸出率下降的原因是________________________________。

(5)反应③的化学方程式是________________________。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是________。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)做电极组成电池,其工作原理为Li4Ti5O12+3LiFePO4
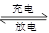 Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。(1)+2
(2)SiO2
(3)TiOCl42—+H2O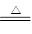 TiO2↓+2H++4Cl-
TiO2↓+2H++4Cl-
(4)温度过高时,反应物氨水(或双氧水)受热易分解
(5)(NH4)2Ti5O15+2LiOH=Li2Ti5O15↓+2NH3·H2O(或2NH3+2H2O)
(6)20?9
(7)LiFePO4-e-=FePO4+Li+
(2)SiO2
(3)TiOCl42—+H2O
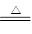 TiO2↓+2H++4Cl-
TiO2↓+2H++4Cl-(4)温度过高时,反应物氨水(或双氧水)受热易分解
(5)(NH4)2Ti5O15+2LiOH=Li2Ti5O15↓+2NH3·H2O(或2NH3+2H2O)
(6)20?9
(7)LiFePO4-e-=FePO4+Li+
(2)钛铁矿中只有SiO2不与盐酸反应,因此滤渣A的成分是SiO2。(3)TiOCl42—转化为TiO2,Ti的化合价不变,发生的是TiOCl42—的水解反应。(5)反应③为LiOH与(NH4)2Ti5O15的复分解反应。(6)根据得失电子守恒,可得关系式:2Fe2+~H2O2~2Fe3+~H2C2O4,则17%双氧水与H2C2O4的质量比= :90=20:9。(7)该电池充电时阳极上LiFePO4发生氧化反应。
:90=20:9。(7)该电池充电时阳极上LiFePO4发生氧化反应。
点拨:本题考查锂离子电池电极材料的制备工艺流程,考查考生对化工流程的综合分析能力。难度较大。
 :90=20:9。(7)该电池充电时阳极上LiFePO4发生氧化反应。
:90=20:9。(7)该电池充电时阳极上LiFePO4发生氧化反应。点拨:本题考查锂离子电池电极材料的制备工艺流程,考查考生对化工流程的综合分析能力。难度较大。

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
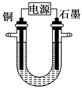

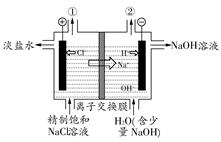
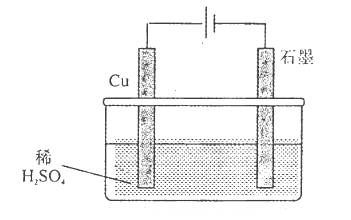
 Cl2↑+H2↑
Cl2↑+H2↑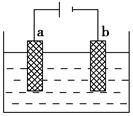
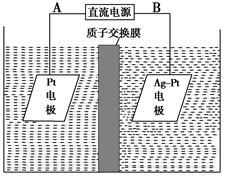
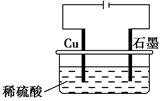
 CuSO4+H2↑
CuSO4+H2↑