题目内容
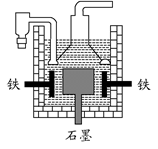
重铬酸钠俗称红矾钠(Na2Cr2O7·2H2O)是重要的化工产品和强氧化剂。工业制备的流程如下:

请回答:
(1)已知Fe(CrO2)2中铬元素是+3价,则Fe(CrO2)2中铁元素是____价。
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成____。
(3)煅烧铬铁矿时,矿石中难溶的Fe(CrO2)2生成可溶于水的Na2CrO4,反应化学方程式如下:

为了加快该反应的反应速率,可采取的措施是____。
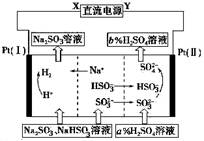
(4)已知CrO42—在不同的酸性溶液中有不同的反应,如:

①往混合溶液甲中加入硫酸必须适量的原因是____。
②混合溶液乙中溶质的化学式是____。
(5)+3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌,所以制取红矾钠后的废水中含有的Cr2O72—必须除去。工业上可用电解法来处理含Cr2O72—的废水,下图为电解装置示意图(电极材料分别为铁和石墨)。通电后,Cr2O72—在b极附近转变为Cr3+,一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去。
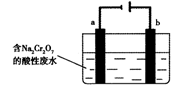
a电极的电极反应式是 ,
b电极附近反应的离子方程式是 。

请回答:
(1)已知Fe(CrO2)2中铬元素是+3价,则Fe(CrO2)2中铁元素是____价。
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成____。
(3)煅烧铬铁矿时,矿石中难溶的Fe(CrO2)2生成可溶于水的Na2CrO4,反应化学方程式如下:

为了加快该反应的反应速率,可采取的措施是____。
(4)已知CrO42—在不同的酸性溶液中有不同的反应,如:

①往混合溶液甲中加入硫酸必须适量的原因是____。
②混合溶液乙中溶质的化学式是____。
(5)+3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌,所以制取红矾钠后的废水中含有的Cr2O72—必须除去。工业上可用电解法来处理含Cr2O72—的废水,下图为电解装置示意图(电极材料分别为铁和石墨)。通电后,Cr2O72—在b极附近转变为Cr3+,一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去。

a电极的电极反应式是 ,
b电极附近反应的离子方程式是 。
(1)+2 (2)FeO?Cr2O3;
(3)粉碎矿石、升高温度;
(4)①加入太少,不能完全除去碳酸钠,过量会生成Na2Cr3O10的副产物②Na2Cr2O7和Na2SO4;
(5)2H++2e-=H2↑,Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.
(3)粉碎矿石、升高温度;
(4)①加入太少,不能完全除去碳酸钠,过量会生成Na2Cr3O10的副产物②Na2Cr2O7和Na2SO4;
(5)2H++2e-=H2↑,Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.
试题分析:(1)根据化合物中化合价代数和为零的原则,铁元素的化合价为+2价
(2)根据铁、铬元素化合价,Fe(CrO2)2可写成FeO?Cr2O3
(3)根据条件对反应速率的影响,适合该反应加快反应速率的条件是粉碎矿石,增大接触面积、升高温度;
(4)①加入硫酸的目的是除去碳酸钠,太少,不能完全除去碳酸钠,过量会生成Na2Cr3O10的副产物②混合物乙溶质的化学式为Na2Cr2O7和Na2SO4;
(5)b为阳极,发生氧化反应,而Cr2O72—在b极附近转变为Cr3+发生了还原反应,所以b为铁,失去电子被氧化为Fe2+;a为石墨,作阴极,所以a极氢离子放电产生氢气,电极反应方程式为2H++2e-=H2↑,Cr2O72—作氧化剂被还原,Fe2+作还原剂,被氧化成Fe3+,结合溶液的酸性环境得离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O

练习册系列答案
相关题目

 4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH
4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH 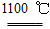 Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )