0 105479 105487 105493 105497 105503 105505 105509 105515 105517 105523 105529 105533 105535 105539 105545 105547 105553 105557 105559 105563 105565 105569 105571 105573 105574 105575 105577 105578 105579 105581 105583 105587 105589 105593 105595 105599 105605 105607 105613 105617 105619 105623 105629 105635 105637 105643 105647 105649 105655 105659 105665 105673 203614
 2NH3(g)
2NH3(g)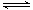 2SO3 (g) ,△H < 0 。如图4是某次实验的化学反应速率随时间变化的图象,推断在t1时刻突然变化的原因可能是( )
2SO3 (g) ,△H < 0 。如图4是某次实验的化学反应速率随时间变化的图象,推断在t1时刻突然变化的原因可能是( )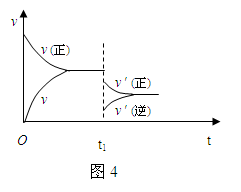
 3H2+N2,测得NH3的分解率为x%。若在其他条件不变时,再充入lmol NH3,待建立新的平衡后,又测得NH3的分解率为y%,则x和y的正确关系为 ( )
3H2+N2,测得NH3的分解率为x%。若在其他条件不变时,再充入lmol NH3,待建立新的平衡后,又测得NH3的分解率为y%,则x和y的正确关系为 ( ) CO(g)+3H2(g) △H1 ②CO(g)+2H2(g)
CO(g)+3H2(g) △H1 ②CO(g)+2H2(g)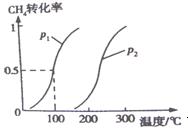
 式为K= ,100℃,压强为p1时平衡常数的值是 。
式为K= ,100℃,压强为p1时平衡常数的值是 。
 3C(g)+4D(g)中,下列情况能够降低该反应速率的是
3C(g)+4D(g)中,下列情况能够降低该反应速率的是