0 105203 105211 105217 105221 105227 105229 105233 105239 105241 105247 105253 105257 105259 105263 105269 105271 105277 105281 105283 105287 105289 105293 105295 105297 105298 105299 105301 105302 105303 105305 105307 105311 105313 105317 105319 105323 105329 105331 105337 105341 105343 105347 105353 105359 105361 105367 105371 105373 105379 105383 105389 105397 203614

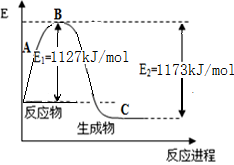

 FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;
FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;