0 105136 105144 105150 105154 105160 105162 105166 105172 105174 105180 105186 105190 105192 105196 105202 105204 105210 105214 105216 105220 105222 105226 105228 105230 105231 105232 105234 105235 105236 105238 105240 105244 105246 105250 105252 105256 105262 105264 105270 105274 105276 105280 105286 105292 105294 105300 105304 105306 105312 105316 105322 105330 203614
 →D→ → → H
→D→ → → H
 1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= .(2分)
1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= .(2分) 液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。
液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。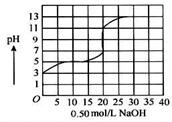
 的浓度是0.15 mol/L
的浓度是0.15 mol/L ol/L的Ba(OH)2溶液,③pH=10的Na2S溶液
ol/L的Ba(OH)2溶液,③pH=10的Na2S溶液 ,④pH=5的NH4NO3溶液中,发生电离的水的物
,④pH=5的NH4NO3溶液中,发生电离的水的物 质的量之比是( )
质的量之比是( )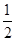 O2(g)=H2O(g);△H=一24l.8kJ/mol下列说法中错误的是
O2(g)=H2O(g);△H=一24l.8kJ/mol下列说法中错误的是