0 104468 104476 104482 104486 104492 104494 104498 104504 104506 104512 104518 104522 104524 104528 104534 104536 104542 104546 104548 104552 104554 104558 104560 104562 104563 104564 104566 104567 104568 104570 104572 104576 104578 104582 104584 104588 104594 104596 104602 104606 104608 104612 104618 104624 104626 104632 104636 104638 104644 104648 104654 104662 203614



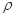 g·cm-3,阿伏加德罗常数为NA,
g·cm-3,阿伏加德罗常数为NA,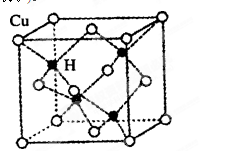
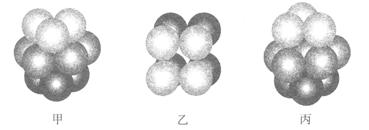
 和黑色的HD两种化合物。
和黑色的HD两种化合物。 中B原子采取的杂化轨道类型为 。
中B原子采取的杂化轨道类型为 。 分子的空间构型为 。
分子的空间构型为 。 极易溶于
极易溶于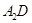 ,原因是 。
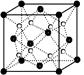
,原因是 。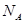 表示阿伏伽德罗常数,晶胞的边长为a。晶胞的高为h,则晶胞的密度可表示为 g/cm3。(用只含r和
表示阿伏伽德罗常数,晶胞的边长为a。晶胞的高为h,则晶胞的密度可表示为 g/cm3。(用只含r和
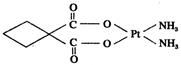
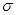 键 G.
键 G.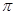 键
键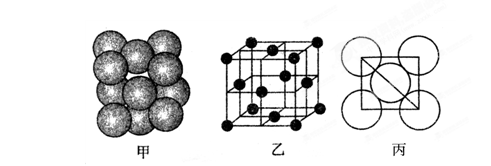
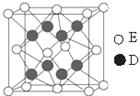
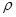 = g/cm3。(用含M、NA、b的计算式表示,不用化简)。
= g/cm3。(用含M、NA、b的计算式表示,不用化简)。