0 103850 103858 103864 103868 103874 103876 103880 103886 103888 103894 103900 103904 103906 103910 103916 103918 103924 103928 103930 103934 103936 103940 103942 103944 103945 103946 103948 103949 103950 103952 103954 103958 103960 103964 103966 103970 103976 103978 103984 103988 103990 103994 104000 104006 104008 104014 104018 104020 104026 104030 104036 104044 203614
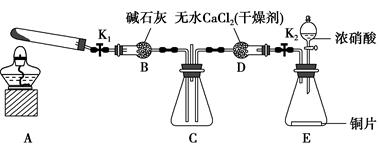
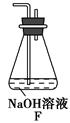
 KCl+2NH3↑
KCl+2NH3↑