题目内容
下列说法中,正确的是( )
| A、金属钠能在氯气中燃烧,生成白色烟雾 |
| B、铜丝在氯气中燃烧,生成蓝绿色的氯化铜 |
| C、点燃是使氯气跟氢气化合的唯一条件 |
| D、氯气跟变价金属反应生成高价金属氯化物 |
考点:钠的化学性质,氯气的化学性质,铜金属及其重要化合物的主要性质
专题:元素及其化合物
分析:A.钠和氯气反应生成氯化钠,为固体观察不到有雾生成;
B.铜丝在氯气中燃烧,生成红棕色的烟;
C.氢气和氯气可在点燃或光照条件下反应;
D.氯气具有强氧化性.
B.铜丝在氯气中燃烧,生成红棕色的烟;
C.氢气和氯气可在点燃或光照条件下反应;
D.氯气具有强氧化性.
解答:
解:A.钠和氯气反应生成氯化钠,为固体,可观察到白烟生成,观察不到有雾生成,雾为小液滴,故A错误;
B.铜丝在氯气中燃烧,生成红棕色的烟,故B错误;
C.氢气和氯气可在点燃或光照条件下反应,光照条件下发生爆炸,故C错误;
D.氯气具有强氧化性,与金属反应生成最高价氯化物,故D正确.
故选D.
B.铜丝在氯气中燃烧,生成红棕色的烟,故B错误;
C.氢气和氯气可在点燃或光照条件下反应,光照条件下发生爆炸,故C错误;
D.氯气具有强氧化性,与金属反应生成最高价氯化物,故D正确.
故选D.
点评:本题考查较为综合,涉及钠、铜、氯气等物质的性质,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大,学习中注意积累.

练习册系列答案
相关题目
用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列操作会引起测定结果偏高的是( )
(1)滴定时,装待测溶液的锥形瓶有少量水;(2)酸式滴定管用蒸馏水洗后,未用标准溶液洗;(3)滴定终点读数时,仰视刻度线.
(1)滴定时,装待测溶液的锥形瓶有少量水;(2)酸式滴定管用蒸馏水洗后,未用标准溶液洗;(3)滴定终点读数时,仰视刻度线.
| A、只有(1) |
| B、只有(2) |
| C、(2)(3) |
| D、(1)(2)(3) |
配制100mL 1.0mol?L-1的Na2CO3溶液,下列情况会导致溶液浓度偏高的是( )
| A、容量瓶使用前用1.0 mol?L-1的Na2CO3溶液润洗 |
| B、配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 |
| C、仰视确定滴定终点 |
| D、用敞开容器称量Na2CO3且时间过长 |
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 物质 组别 | 甲 | 乙 | 丙 |
| A | Al2O3 | HCl | NaOH |
| B | SiO2 | NaOH | HF |
| C | HCl | NaOH | NaHCO3 |
| D | NH3 | O2 | HNO3 |
| A、A | B、B | C、C | D、D |
下列有关物质性质的应用错误的是( )
| A、钠具有很强的还原性,可用钠与TiCl4反应制取钛 |
| B、通过铝热反应可以用来焊接钢轨 |
| C、过氧化钠可以与CO2、H2O反应,可用作潜水艇供氧剂 |
| D、Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 |
下列各组离子,能在溶液中大量共存的是( )
| A、H+、Fe3+、Cl-、CO32- |
| B、K+、Na+、Br-、NO3- |
| C、NH4+、K+、OH-、SO42- |
| D、Ag+、Na+、Cl-、K+ |
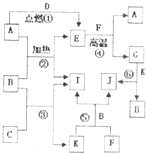 如图是中学化学常见物质之间的转换关系,其中A、C、D、F、I为单质,其余为化合物,C和D在点燃或者加热的条件下生成淡黄色的固体,B常温下为液态.试回答下列有关问题:
如图是中学化学常见物质之间的转换关系,其中A、C、D、F、I为单质,其余为化合物,C和D在点燃或者加热的条件下生成淡黄色的固体,B常温下为液态.试回答下列有关问题: