题目内容
一定条件下,在固定体积的密闭容器中发生反应2NH3(g)?N2(g)+3H2(g)△H>0并达平衡后,仅改变下表中反应条件x,该平衡体系中随x的递增而y递减的是( )
| 选项 | A | B | C | D |
| x | 加入H2的物质的量 | 温度 | 温度 | 加入NH3的物质的量 |
| y | NH3的转化率 | 逆反应的反应速率 | 平衡常数K | 体系中混合气的密度 |
| A、A、 | B、B、 | C、C、 | D、D、 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:正反应吸热,则升高温度平衡向正反应方向移动,结合浓度对平衡移动的影响判断.
解答:
解:正反应吸热,则升高温度平衡向正反应方向移动,NH3的物质的量减小,平衡常数增大,逆反应的反应速率也增大,则B、C错误;
加入H2的物质的量,平衡向逆反应方向移动,则NH3的转化率减小,故A正确;
加入NH3的物质的量,生成物物质的量总和增大,体积也没变,所以体系中混合气的密度也增大,故D错误,
故答案为:A.
加入H2的物质的量,平衡向逆反应方向移动,则NH3的转化率减小,故A正确;
加入NH3的物质的量,生成物物质的量总和增大,体积也没变,所以体系中混合气的密度也增大,故D错误,
故答案为:A.
点评:本题考查外界条件对平衡状态的影响以及平衡状态的判断,题目难度中等,注意相关知识的把握

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中,正确的是( )
| A、金属钠能在氯气中燃烧,生成白色烟雾 |
| B、铜丝在氯气中燃烧,生成蓝绿色的氯化铜 |
| C、点燃是使氯气跟氢气化合的唯一条件 |
| D、氯气跟变价金属反应生成高价金属氯化物 |
化学无处不在,下列与化学有关的说法不正确的是( )
| A、可用蘸浓硫酸的棉花棒检验输送氨气的管道是否漏气 |
| B、“地沟油”禁止食用,但可用来制肥皂 |
| C、从海水中提取物质都必须经过化学反应才能实现 |
| D、侯式制碱法的工艺过程中应用了物质溶液度的差异 |
下列各组物质中前者为电解质、后者属于非电解质的是( )
| A、CaO、C2H5OH |
| B、HCl、CH3COOH |
| C、H2S、BaSO4 |
| D、NH3?H2O、Cu |
温室效应产生的原因之一是大气中CO2的含量剧增,要想减缓这一现象的发生,最理想的燃料是( )
| A、天然气 | B、氢气 |
| C、液化石油气 | D、酒精 |
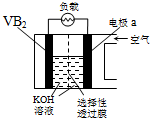 硼化钒(VB2)-空气电池能力最高的电池,电池示意图如下,该电池工作时反应为:4VB2+11O2→4B2O3+2V2O5.下列说法正确的是( )
硼化钒(VB2)-空气电池能力最高的电池,电池示意图如下,该电池工作时反应为:4VB2+11O2→4B2O3+2V2O5.下列说法正确的是( )| A、电极a为电池负极 |
| B、图中选择性透过膜只能让阳离子选择性透过 |
| C、电子由VB2极经KOH溶液流向a电极 |
| D、VB2极发生的电极反应为:2VB2+22OH--22e-→V2O5+2B2O3+11H2O |
下列离子方程式正确的是( )
| A、醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B、碘水中通入足量的SO2:I2+SO2+2H2O=2HI+SO42-+2H+ |
| C、NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、4 mol?L-1的NaAlO2溶液和7 mol?L-1的盐酸溶液等体积混合均匀4AlO2-+7H++H2O=3A1(OH)3↓+Al3+ |
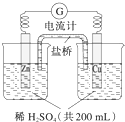 由锌片、铜片和200mL稀H2SO4组成的原电池如图所示.
由锌片、铜片和200mL稀H2SO4组成的原电池如图所示.