题目内容
某学习小组先向试管中加入3ml蒸馏水,滴人酚酞试液,再向试管中倒入1ml煤油,然后从试剂瓶中取出一块金属钠,用小刀切一小块放入试管中,可观察到钠首先沉到煤油底部,一接触水即产生大量气泡,钠块变成球状向上浮,同时水层变红色,一会儿之后,钠又慢慢沉降到两种液体的交界处,又立即产生大量气泡,使钠上浮,如此反复,
直至钠块消失.根据上述描述回答下列问题:
(1)本文中说明的钠的物理性质主要有:
①
②
③ ;
(2)0.23g钠投入20ml水中完全反应放出气体标况下的体积是 mL,所得溶液的质量分数是%(保留两位小数) ,所得溶液物质的量浓度是 mol?L-1(水的密度是1g/cm3,不计溶液体积变化).
直至钠块消失.根据上述描述回答下列问题:
(1)本文中说明的钠的物理性质主要有:
①
②
③
(2)0.23g钠投入20ml水中完全反应放出气体标况下的体积是
考点:钠的化学性质
专题:金属概论与碱元素
分析:(1)物理性质包含:色、态、味、熔沸点、密度、硬度等;
(2)根据钠和氢气之间的关系式计算氢气体积;根据原子守恒计算氢氧化钠的质量,溶液的质量等于氢氧化钠的质量和水的质量.
(2)根据钠和氢气之间的关系式计算氢气体积;根据原子守恒计算氢氧化钠的质量,溶液的质量等于氢氧化钠的质量和水的质量.
解答:
解:(1)物理性质包含:色、态、味、熔沸点、密度、硬度等,通过以上实验知,钠的性质有:硬度小、熔点低、密度介于水和煤油之间,故答案为:①硬度小;②熔点低;③密度介于水和煤油之间;
(2)根据2Na+2H2O=H2↑+2NaOH知,生成气体体积=
×22.4L/mol×
=112mL,根据原子守恒得n(NaOH)=n(Na)=0.01mol,m(NaOH)=0.01mol×40g/mol=0.4g,溶液质量=0.23g+20g-
×1×2g/mol=20.22g,质量分数=
×100%=1.98%,C(NaOH)=
=0.5mol/L,
故答案为:112;1.98%;0.5.
(2)根据2Na+2H2O=H2↑+2NaOH知,生成气体体积=
| 0.23g |
| 23g/mol |
| 1 |
| 2 |
| ||
| 2 |
| 0.4g |
| 20.22g |
| 0.01mol |
| 0.02L |
故答案为:112;1.98%;0.5.
点评:本题考查了钠的性质,根据钠和水的反应再结合质量分数、物质的量浓度的计算方法解答即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
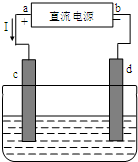 与图有关的下列叙述正确的是( )
与图有关的下列叙述正确的是( )| A、a为直流电源的负极 |
| B、用该装置制白铁(镀锌铁),d为铁电极 |
| C、用该装置精炼铜,d为粗铜电极 |
| D、c、d均为石墨电极电解饱和食盐水时,c电极附近pH升高 |
某化合物X受热分解的化学方程式为:2X=A↑+2B↑+4C↑,在一定条件下,测得生成物混合气体对氢气的相对密度为11.43,则相同条件下化合物X的相对分子质量为( )
| A、11.43 |
| B、80.01 |
| C、22.86 |
| D、160.02 |

 甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景. 完成以下三个小题
完成以下三个小题
