题目内容
由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转换关系,工业上电解熔融的甲可制取金属A.请回答:

(1)写出下列物质的化学式:A 、甲 .
(2)写出乙物质的溶液中通入过量CO2的现象: ;
(3)写出丁与过量氨水反应的离子方程式: .

(1)写出下列物质的化学式:A
(2)写出乙物质的溶液中通入过量CO2的现象:
(3)写出丁与过量氨水反应的离子方程式:
考点:无机物的推断
专题:推断题
分析:A是金属单质,A能和NaOH溶液反应生成乙和C,则A是Al,Al和NaOH溶液反应生成NaAlO2和H2,C是单质、乙是化合物,所以C是H2、乙是NaAlO2;
工业上电解熔融的甲可制取金属Al,工业上用电解氧化铝的方法冶炼Al,所以A甲是Al2O3,Al和氧气反应生成
Al2O3,所以B是O2,Al2O3和HCl反应生成AlCl3和H2O,Al2O3和NaOH溶液反应生成NaAlO2和H2O,则丙是H2O、丁是AlCl3,氯化铝和氨水反应生成氢氧化铝、氯化铵,偏铝酸钠和二氧化碳反应生成碳酸氢钠、氢氧化铝,所以戊是Al(OH)3,结合物质的性质分析解答.
工业上电解熔融的甲可制取金属Al,工业上用电解氧化铝的方法冶炼Al,所以A甲是Al2O3,Al和氧气反应生成
Al2O3,所以B是O2,Al2O3和HCl反应生成AlCl3和H2O,Al2O3和NaOH溶液反应生成NaAlO2和H2O,则丙是H2O、丁是AlCl3,氯化铝和氨水反应生成氢氧化铝、氯化铵,偏铝酸钠和二氧化碳反应生成碳酸氢钠、氢氧化铝,所以戊是Al(OH)3,结合物质的性质分析解答.
解答:
解:A是金属单质,A能和NaOH溶液反应生成乙和C,则A是Al,Al和NaOH溶液反应生成NaAlO2和H2,C是单质、乙是化合物,所以C是H2、乙是NaAlO2;
工业上电解熔融的甲可制取金属Al,工业上用电解氧化铝的方法冶炼Al,所以A甲是Al2O3,Al和氧气反应生成Al2O3,所以B是O2,Al2O3和HCl反应生成AlCl3和H2O,Al2O3和NaOH溶液反应生成NaAlO2和H2O,则丙是H2O、丁是AlCl3,氯化铝和氨水反应生成氢氧化铝、氯化铵,偏铝酸钠和过量二氧化碳反应生成碳酸氢钠、氢氧化铝,所以戊是Al(OH)3,
(1)通过以上分析知,A是Al,甲是Al2O3,故答案为:Al;Al2O3;
(2)偏铝酸钠和过量二氧化碳反应生成NaHCO3和Al(OH)3,Al(OH)3不溶于水,所以乙物质的溶液中通入过量CO2的现象是:溶液变浑浊,故答案为:溶液变浑浊;
(3)氯化铝和氨水反应生成氢氧化铝、氯化铵,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3 NH4+
,故答案为:Al3++3NH3?H2O=Al(OH)3↓+3 NH4+.
工业上电解熔融的甲可制取金属Al,工业上用电解氧化铝的方法冶炼Al,所以A甲是Al2O3,Al和氧气反应生成Al2O3,所以B是O2,Al2O3和HCl反应生成AlCl3和H2O,Al2O3和NaOH溶液反应生成NaAlO2和H2O,则丙是H2O、丁是AlCl3,氯化铝和氨水反应生成氢氧化铝、氯化铵,偏铝酸钠和过量二氧化碳反应生成碳酸氢钠、氢氧化铝,所以戊是Al(OH)3,
(1)通过以上分析知,A是Al,甲是Al2O3,故答案为:Al;Al2O3;
(2)偏铝酸钠和过量二氧化碳反应生成NaHCO3和Al(OH)3,Al(OH)3不溶于水,所以乙物质的溶液中通入过量CO2的现象是:溶液变浑浊,故答案为:溶液变浑浊;
(3)氯化铝和氨水反应生成氢氧化铝、氯化铵,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3 NH4+
,故答案为:Al3++3NH3?H2O=Al(OH)3↓+3 NH4+.
点评:本题以铝及其化合物为载体考查了物质间的转化及物质的推断,明确铝及其化合物的性质是解本题关键,根据铝的性质及工业上冶炼铝的原料为突破口采用正逆结合的方法推断,将铝及其化合物的知识总结归纳而形成知识网络,灵活运用,注意:氢氧化铝能溶于强碱但不溶于弱碱.

练习册系列答案
相关题目
下列措施符合环保要求的是( )
| A、废旧电池不随意乱扔,放在普通垃圾箱中 |
| B、在农田里焚烧树叶、稻草、垃圾等,既可以清洁环境,灰烬又可以作肥料 |
| C、固体煤不直接使用,而是汽化或液化后作燃料 |
| D、燃放烟花爆竹 |

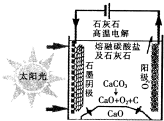 资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业