��Ŀ����
15����10L�����ܱ������г���A��g����B��g����������ӦA��g��+B��g��?2C��g��+D��s��������ʵ���������±�������˵����ȷ���ǣ�������| ʵ���� | �¶�/�� | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | |
| n��A�� | n��B�� | n��C�� | ||
| �� | 700 | 4.0 | 1.0 | 1.80 |
| �� | 800 | 1.0 | 4.0 | 1.60 |
| �� | 800 | 2.0 | 2.0 | a |
| �� | 900 | 1.0 | 1.0 | b |
| A�� | ʵ����У���10min�ﵽƽ�⣬��v��D��=9.0��10-2mol/��L•min�� | |
| B�� | ʵ����У��÷�Ӧ��ƽ�ⳣ��K=3.2 | |
| C�� | ʵ����У��ﵽƽ��ʱA��ת����Ϊ60% | |
| D�� | ʵ����У��ﵽƽ��ʱ��b��1.0 |
���� A���ﵽƽ��״̬����C���ʵ���Ϊ1.8mol�����ݻ�ѧ����ʽ����õ�����DΪ0.9mol����Ӧ����=$\frac{��c}{��t}$��
B�����ݻ�ѧƽ�����м�����ʽ����ƽ��Ũ�ȣ�ƽ�ⳣ������������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ���ݴη��˻��õ���
C��ʵ��ڢ���ͬ�¶��½��еķ�Ӧ��ƽ�ⳣ�����䣬������м�����ʽ����ת���ʣ�
D���٢����ݷ�����֪�¶�����C���ʵ�����С��˵������ӦΪ���ȷ�Ӧ���¶�����ƽ��������У���Ͷ������800��C���м���õ�b��Ȼ������ƽ���ƶ��жϣ�
��� �⣺A���ﵽƽ��״̬����C���ʵ���Ϊ1.8mol�����ݻ�ѧ����ʽ����õ�����DΪ0.9mol����Ӧ����=$\frac{��c}{��t}$=$\frac{\frac{1.80mol}{10L}}{10min}$=0.018mol/L•min����A����
B�����ݻ�ѧƽ�����м�����ʽ����ƽ��Ũ�ȣ�
A��g��+B��g��?2C��g��+D��s��
��ʼ����mol/L�� 0.1 0.4 0 0
�仯����mol/L�� 0.08 0.08 0.16 0.08
ƽ������mol/L�� 0.02 0.32 0.16 0.08
K=$\frac{0.1{6}^{2}}{0.02��0.32}$=4����B����
C��ʵ��ڢ���ͬ�¶��½��еķ�Ӧ��ƽ�ⳣ�����䣬���ݻ�ѧƽ�����м�����ʽ����ƽ��Ũ�ȣ�
A��g��+B��g��?2C��g��+D��s��
��ʼ����mol/L�� 0.2 0.2 0
�仯����mol/L�� 0.05a 0.05a 0.1a
ƽ������mol/L�� 0.2-0.05a 0.2-0.05a 0.1a
K=$\frac{��0.1a��^{2}}{��0.2-0.05a��^{2}}$
a=2mol��ʵ����У��ﵽƽ��ʱA��ת����=$\frac{0.05��2mol/L}{0.2mol/L}$=50%��
��C����
D��ʵ�������ʼ���ͷ�Ӧ�۱Ƚϼ�����һ��������800��C������C�����ʵ���b=1mol���٢����ݷ�����֪�¶�����C���ʵ�����С��˵������ӦΪ���ȷ�Ӧ��ʵ������¶�����ƽ��������У��ﵽƽ��ʱ��b��1.0����D��ȷ��
��ѡD��
���� ���⿼���˻�ѧƽ�⡢��ѧ��Ӧ����Ӱ�����ء���ѧƽ����㡢���ݷ����жϵ�֪ʶ�����ջ����ǽ���ؼ�����Ŀ�ѶȽϴ�

| ���� | HCOOH | HClO | H2CO3 | H2SO3 |
| ���볣�� ��25�棩 | Ki=1.77��10-4 | Kii=2.98��10-6 | K1Ki1=4.3��10-7 Ki2=5.6��10-11 | Ki1=1.54��10-2 Ki2=5.6��10-7 |
��2��1molCl2��2molNa2CO3��aq����Ӧ������NaCl���NaHCO3��NaClO���ѧʽ����
��3����һ������NaHCO3��aq����ͨ��������SO2��g������Ӧ�����ӷ���ʽΪHCO3-+SO2��HSO3-+CO2����
�����ᣨH2SeO3��Ҳ��һ�ֶ�Ԫ���ᣬ��������һ����ɫ���壬������ˮ���н�ǿ�������ԣ�
��4�����������������ع��ȿ��Ƶ����ᣨH2SeO4������ƽ�÷�Ӧ����ʽ�����������ת��
�ķ������Ŀ��
5H2SeO3+2KMnO4��1K2SeO4+2MnSeO4+2H2SeO4+3H2O
��5������ͬ���Ԫ��Te������������ˮ�������ᣨH6TeO6�������Ա�H2SO4����ѡ�ǿ�������������������Ա�����ǿ����������ͨ��SO2���壬����Ӧ�����ɵ�TeO2��Te�����ʵ���֮��Ϊ2��1��д���÷�Ӧ�Ļ�ѧ����ʽ5SO2+3H6TeO6��2TeO2+Te+5H2SO4+4H2O����6mol������һ����SO2ǡ����ȫ��Ӧ��������Һ���Ϊ20L����������Һ��pHΪ0��
 �ҹ�֧�֡����İ��ˡ���һ����Ҫ�����Ǽ�������˶�Ա�����˷ܼ���ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵����ȷ���ǣ�������
�ҹ�֧�֡����İ��ˡ���һ����Ҫ�����Ǽ�������˶�Ա�����˷ܼ���ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵����ȷ���ǣ�������| A�� | ���������ڷ����廯���� | |
| B�� | ���л���ķ���ʽΪC15H18O3 | |
| C�� | ��FeCl3��Һ����ɫ����Ϊ�������뱽������ͬϵ�� | |
| D�� | 1mol�û����������뺬3molBr2����ˮ������Ӧ |
| ��� | Ũ������ˮ������� | ʵ �� �� �� |
| �� | 1�s1 | ��Ӧ���ʿ죬��Һ�ܿ�����ɫ��ͭ˿�����д�������ð��������ʺ���ɫ |
| �� | 1�s3 | ��Ӧ���ʽϿ죬��Һ�����ɫ��ͭ˿�����д�������ð����������ɫ |
| �� | 1�s5 | ��Ӧ���������Ⱥ����ʼӿ죬��Һ�����ɫ��ͭ˿����������ð����������ɫ |
��2����ȤС����ľ̿��Ũ����Ϊ��ʼԭ�ϣ�̽��һ��������������Ʒ�Ӧ�Ʊ��������ƣ����װ�����£�����װ���п�����Ӱ�죩����ش��������⣺

����װ������������е�һ������ǣ����װ�õ������ԣ�
���Ʋ�B�п��Թ۲쵽����Ҫ�����ǣ�ͭƬ���ܽ⣬��Һ������������ɫ���ݣ�Cװ�õ������ǣ���ȥNO�л��е�CO2��
��װ��D�г�����NaNO2�⣬������һ�ֹ�̬����Y��Y�Ļ�ѧʽ�ǣ�NaOH������ͨ���ʵ��Ľ���������Y���ʣ���������Ľ���������װ�м�ʯ�ҵĸ���ܴ���Cװ�ã�
��Eװ�õ�ʵ��Ŀ���ǣ�β����������ֹ�к�����Դ�����Ⱦ��
| A�� | K��F | B�� | Na��Cl | C�� | Al��S | D�� | Mg��Cl |
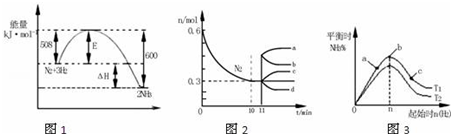
| A�� | ��ͼ1��֪2NH3��g��?N2��g��+3H2��g����H=-92kJ•mol-1 | |
| B�� | ͼ2��0��10min�ڸ÷�Ӧ��ƽ������v��H2��=0.045mol•L-1•min-1����11min�������������䣬ѹ�����������Ϊ1L����n��N2���ı仯����Ϊd | |
| C�� | ͼ3��a��b��c����������ƽ��״̬�У���Ӧ��N2��ת������ߵ���b�� | |
| D�� | ͼ3��T1��T2��ʾ�¶ȣ���Ӧ�¶��µ�ƽ�ⳣ��ΪK1��K2����T1��T2��K1��K2 |