题目内容
下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
| A、液溴和苯分别受热变为气体 |
| B、干冰和氯化铵分别受热变为气体 |
| C、二氧化硅和铁分别受热熔化 |
| D、食盐和葡萄糖分别溶解在水中 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:物质发生变化时,所克服的粒子间相互作用属于同种类型,说明两种晶体的晶体类型相同,导致变化时克服作用力相同,根据晶体类型判断即可.
解答:
解:A.溴和苯都是分子晶体,由液态转化为气体克服分子间作用力,故A正确;
B.干冰属于分子晶体,转化为气体克服分子间作用力,氯化铵是离子晶体,转化为气体时克服离子键,故B错误;
C.二氧化硅属于原子晶体,熔融时克服化学键,铁属于金属晶体,熔融时克服金属键,故C错误;
D.食盐属于离子晶体,溶于水克服离子键,葡萄糖属于分子晶体,溶于水克服分子间作用力,故D错误;
故选A.
B.干冰属于分子晶体,转化为气体克服分子间作用力,氯化铵是离子晶体,转化为气体时克服离子键,故B错误;
C.二氧化硅属于原子晶体,熔融时克服化学键,铁属于金属晶体,熔融时克服金属键,故C错误;
D.食盐属于离子晶体,溶于水克服离子键,葡萄糖属于分子晶体,溶于水克服分子间作用力,故D错误;
故选A.
点评:本题考查化学键及晶体类型的关系,侧重考查基本理论,明确晶体构成微粒是解本题关键,会根据物质的构成微粒确定晶体类型,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在523K时,有以下反应:2HCl(g)+CrO3(g)═CrO2Cl2(g)+H2O(g)+Q (Q>0),反应进行至第5min时,改变某个条件,当反应进行至第10min时,发现生成CrO2Cl2(g)的速率增大,CrO2Cl2的百分含量也增大,则改变的条件不可能是( )
| A、加热 | B、使用催化剂 |
| C、加压 | D、分离出水气 |
钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为W(s)+2I2(g)
WI4(g).下列说法正确的是( )
| 1400℃ |
| 约3000℃ |
| A、温度越高,灯丝的使用寿命越长 |
| B、WI4在灯丝上分解,产生的W又沉积在灯丝上 |
| C、WI4在灯管壁上分解,使灯管的寿命延长 |
| D、温度升高时,WI4的分解速率加快,W和I2的化合速率减慢 |
关于如图所示的原电池,下列说法正确的是 ( )
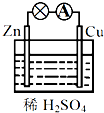

| A、锌棒为正极 |
| B、铜棒上发生还原反应 |
| C、正极反应为Cu-2e-=Cu2+ |
| D、电流从锌棒经外电路流向铜棒 |
下列化合物含有离子键的是( )
| A、H2O |
| B、NH3 |
| C、CaCl2 |
| D、CH4 |
基因测序研究中,常用
P作标记物,下列关于
P的说法正确的是( )
32 15 |
32 15 |
| A、质子数为32 |
| B、质量数为15 |
| C、32P与33P互为同位素 |
| D、中子数为15 |
下列属于放热反应的是( )
| A、生石灰和水 |
| B、碳酸钙高温分解 |
| C、灼热的碳和二氧化碳 |
| D、Ba(OH)2?8H2O晶体和NH4Cl |

