题目内容
11.将20mL 0.3mol/L AgNO3溶液与10mL0.4mol/L CaC12 溶液混合,所得溶液中离子浓度关系正确的是( )| A. | c(Ca2+)>c(Cl-)>c ( NO3-) | B. | c(Ca2+)>c ( NO3-)>c (Cl-) | ||
| C. | c(NO3-)>c ( Ca2+ )>c ( Cl-) | D. | c ( Cl-)>c(Ca2+)>c(NO3-) |
分析 n( AgNO3)=0.3mol/L×0.02L=0.006mol,n(Cl-)=0.4mol/L×0.01L×2=0.008mol,二者发生反应Ag++Cl-=AgCl↓,根据离子方程式知,Ag+完全反应,溶液中还剩余0.002molCl-,再结合物料守恒判断.
解答 解:n( AgNO3)=0.3mol/L×0.02L=0.006mol,n(Cl-)=0.4mol/L×0.01L×2=0.008mol,二者发生反应Ag++Cl-=AgCl↓,根据离子方程式知,Ag+完全反应,溶液中还剩余0.002molCl-,NO3-、Ca2+不反应,n(NO3-)=0.006mol、n(Ca2+)=0.4mol/L×0.01L=0.004mol、n(Cl-)=0.002mol,所以离子浓度大小顺序是c(NO3-)>c ( Ca2+ )>c ( Cl-),故选C.
点评 本题考查离子浓度大小比较,为高频考点,明确离子发生的反应是解本题关键,再结合物料守恒判断,为易错题.

练习册系列答案
相关题目
15.用氢氧化钠固体配制0.10mol/L的氢氧化钠溶液,下列说法中不正确的是( )
| A. | 定容时俯视容量瓶刻度线,会造成所配溶液浓度偏大 | |
| B. | 定容摇匀后发现液面下降,不应再加蒸馏水 | |
| C. | 称量时托盘上要垫上干净的称量纸 | |
| D. | 移液时不慎有部分液体溅出,会造成所配溶液浓度偏小 |
2.当今国际能源研究的热点之一是寻找新能源,下列能源不属于新能源的是( )
| A. | 太阳能 | B. | 氢能 | C. | 风能 | D. | 天然气 |
19.下列氧化还原反应中电子转移情况分析正确的是( )
| A. |  | B. | 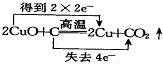 | ||
| C. |  | D. |  |
6.下列关于电解质的说法中正确的是( )
| A. | 纯水的导电性很差,所以水不是电解质 | |
| B. | SO2水溶液的导电性很好,所以SO2是电解质 | |
| C. | 熔融状态时铜的导电性很好,所以铜是电解质 | |
| D. | 硝酸钾在水中和熔融状态时都能导电,所以硝酸钾是电解质 |
16.下列反应的离子方程式正确的是( )
| A. | 碳酸钙溶于醋酸 CaCO3+2H+=Ca2++CO2↑+H2O | |
| B. | 氢氧化钠溶液吸收二氧化硫气体 SO2+2OHˉ=SO42ˉ+H2O | |
| C. | 氯气溶于水 Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氯化铁溶液溶解铜 Cu+2Fe3+=Cu2++2Fe2+ |
3.下列说法不正确的是( )
| A. | 用镊子夹取金属钠固体,切割取用后剩余的钠必须放回原试剂瓶中 | |
| B. | 探究温度对化学反应速率影响时,先将硫代硫酸钠与硫酸两种溶液混合后再用水浴加热 | |
| C. | 金属镁因保存不当造成失火可用细沙盖灭,不能用泡沫灭火器 | |
| D. | 在分液操作中,当试液分层后,打开旋塞,将下层液体放出,然后关闭旋塞,将上层液体从上口倒出 |
20.金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是( )
| A. | 阳极发生还原反应,其电极反应式:Ni2++2e-═Ni | |
| B. | 电解后,电解槽底部的阳极泥中只有Pt | |
| C. | 电解后,溶液中存在的阳离子只有Fe2+和Zn2+ | |
| D. | 电解过程中,阳极质量的减少与阴极质量的增加不相等 |
1.与3.2gSO2所含的氧原子数相等的CO2的质量为( )
| A. | 2.2g | B. | 4.4g | C. | 44g | D. | 22g |