题目内容
25.00ml未知浓度的HNO3溶液与24.18ml 0.6120mol/L的KOH溶液恰好完全中和,试计算HNO3的物质的量浓度.25.00ml这种溶液里含HNO3的质量是多少克?
【答案】分析:根据硝酸和氢氧化钾反应的化学方程式以及公式n=cv、m=nM列表达式计算即可.
解答:解:设硝酸的物质的量浓度是x,据题意得
HNO3 +KOH=H2O+KNO3
1 1
0.025x 0.02418×0.6120
即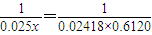
解得x=0.5919mol/L
25.00ml这种溶液里含HNO3的质量m=nM=(0.02418×0.6120)mol×63g/mol=0.93g.
答:HNO3的物质的量浓度为0.5919mol/L,25.00ml这种溶液里含HNO3的质量是0.93克.
点评:本题考查学生利用化学方程式结合物质的量来计算方年的基本知识,属于基本知识考查,较简单.
解答:解:设硝酸的物质的量浓度是x,据题意得
HNO3 +KOH=H2O+KNO3
1 1
0.025x 0.02418×0.6120
即
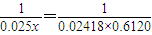
解得x=0.5919mol/L
25.00ml这种溶液里含HNO3的质量m=nM=(0.02418×0.6120)mol×63g/mol=0.93g.
答:HNO3的物质的量浓度为0.5919mol/L,25.00ml这种溶液里含HNO3的质量是0.93克.
点评:本题考查学生利用化学方程式结合物质的量来计算方年的基本知识,属于基本知识考查,较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
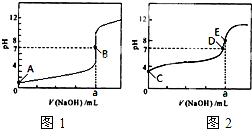
 Ⅰ.室温时1L 0.01mol?L-1的硫酸氢钠溶液的pH为
Ⅰ.室温时1L 0.01mol?L-1的硫酸氢钠溶液的pH为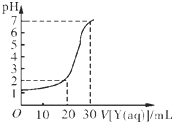 某学生用NaOH标准溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
某学生用NaOH标准溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步: