题目内容
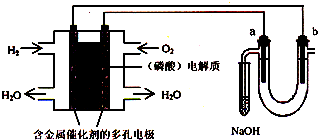
用酸性氢氧燃料电池电解苦卤水 (含Cl-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极).下列说法中,正确的是( )

| A、电池工作时,正极反应式为:O2+2 H2O+4e-=4OH- |
| B、忽略能量损耗,当电池中消耗0.02g H2时,a极周围会产生0.02g H2 |
| C、电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D、电解时,a 电极周围首先放电的是Br-而不是Cl-,说明当其它条件相同时Br-的还原性强于Cl- |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、氢氧燃料电池中,正极上放电的是氧气;
B、燃料电池和电解池中转移的电子数是相等的;
C、电子在导线中移动,不能在溶液中移动;
D、还原性:Br->Cl-,还原性强的离子在阳极先放电.
B、燃料电池和电解池中转移的电子数是相等的;
C、电子在导线中移动,不能在溶液中移动;
D、还原性:Br->Cl-,还原性强的离子在阳极先放电.
解答:
解:A、氢氧燃料电池中,正极上放电的是氧气,在酸性电解质环境下,电极反应式为:O2+4H++4e-═2H2O,故A错误;
B、燃料电池和电解池中转移的电子数是相等的,当电池中消耗0.02gH2,根据电极反应:H2→2H++2e-,所以转移电子0.02mol,b极的电极反应为:2H++2e-→H2,转移电子0.02mol,会产生0.02gH2,故B错误;
C、电子在导线中移动,不能在溶液中移动,故C错误;
D、还原性强的离子在阳极先放电,电解时,a电极周围首先放电的是Br-而不是Cl-,所以还原性为Br->Cl-,故D正确.
故选D.
B、燃料电池和电解池中转移的电子数是相等的,当电池中消耗0.02gH2,根据电极反应:H2→2H++2e-,所以转移电子0.02mol,b极的电极反应为:2H++2e-→H2,转移电子0.02mol,会产生0.02gH2,故B错误;
C、电子在导线中移动,不能在溶液中移动,故C错误;
D、还原性强的离子在阳极先放电,电解时,a电极周围首先放电的是Br-而不是Cl-,所以还原性为Br->Cl-,故D正确.
故选D.
点评:本题考查了原电池和电解池,明确原电池和电解池原理是解本题关键,把握离子的放电顺序,注意电子不进入电解质溶液,溶液中阴阳离子定向移动而形成电流,难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
已知:①CO(g)+1/2O2(g)=CO2(g)△H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(l)△H2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H3=-1370kJ/mol.
则2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的△H为( )
②H2(g)+1/2O2(g)=H2O(l)△H2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H3=-1370kJ/mol.
则2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的△H为( )
| A、-339.2 kJ/mol |
| B、-1983.8kJ/mol |
| C、+518.2kJ/mol |
| D、-801.2kJ/mol |
下列说法中正确的是( )
| A、保鲜膜、一次性食品袋的主要成分是聚氯乙烯 |
| B、电解食盐水,不能用铁等做电极,否则得不到氯气 |
| C、稻草不可能转化成葡萄糖 |
| D、通过丁达尔现象可以区分氯化铁溶液与氢氧化铁胶体 |
已知下列热化学方程式:2H2O(g)═2H2(g)+O2(g)△H=+483.6kJ/mol,2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol.当1g水由液态变为气态时,其热量变化是( )
①吸热 ②放热 ③2.44kJ ④88kJ.
①吸热 ②放热 ③2.44kJ ④88kJ.
| A、①④ | B、②④ | C、①③ | D、②③ |
已知:C(s)+O2(g)=CO2(g);△H=-393.5kJ/mol
H2(g)+
O2(g)=H2O(l);△H=-241.8kJ/mol
欲得到相同的热量,需分别燃烧固体碳和氢气的质量比约为( )
H2(g)+
| 1 |
| 2 |
欲得到相同的热量,需分别燃烧固体碳和氢气的质量比约为( )
| A、2:3.25 |
| B、12:3.25 |
| C、1:1 |
| D、393.5:241 |
苯环实际上不具有碳碳单键和双键的简单交替结构,可以作为证据的事实有( )
| A、苯的间位二元取代物只有-种 |
| B、苯的邻位二元取代物只有一种 |
| C、苯不能使酸性KMnO4溶液褪色 |
| D、苯能在加热和催化剂存在的条件下与氯气加成生成环已烷 |
下列一定没有伴随化学变化的是( )
| A、电解质溶液导电 |
| B、活性炭使品红褪色 |
| C、钢铁缓慢氧化 |
| D、酚酞遇碱变红 |
体积相同的甲乙两容器中,一个充满HCl,另一个充满H2和Cl2的混合气体.同温、同压下,两个容器内的气体一定具有相同的( )
| A、原子总数 | B、分子总数 |
| C、质量 | D、密度 |

 官能团名称
官能团名称