题目内容
下列叙述正确的是( )
| A、氯化氢水溶液能导电,所以氯化氢是电解质 |
| B、铜丝能导电,所以铜是电解质 |
| C、固体氢氧化钠不导电,所以氢氧化钠是非电解质 |
| D、SO3溶于水能导电,所以SO3是电解质 |
考点:电解质与非电解质
专题:离子反应专题
分析:水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物不管在水溶液中或熔融状态下能够导电与否,都不是电解质也不是非电解质.
解答:
解:A、氯化氢的水溶液能导电,所以氯化氢是电解质,故A正确.
B、无论电解质还是非电解质都必须是化合物,铜丝是单质不是化合物,所以铜丝既不是电解质也不是非电解质,故B错误.
C、氯化钠固体没有自由移动的离子,所以不导电,但氯化钠的水溶液能导电,所以氯化钠是电解质,故C错误.
D、三氧化硫的水溶液导电,电离出自由移动离子的物质是硫酸不是三氧化硫,所以三氧化硫是非电解质,故D错误.
故选A.
B、无论电解质还是非电解质都必须是化合物,铜丝是单质不是化合物,所以铜丝既不是电解质也不是非电解质,故B错误.
C、氯化钠固体没有自由移动的离子,所以不导电,但氯化钠的水溶液能导电,所以氯化钠是电解质,故C错误.
D、三氧化硫的水溶液导电,电离出自由移动离子的物质是硫酸不是三氧化硫,所以三氧化硫是非电解质,故D错误.
故选A.
点评:本题考查了电解质和非电解质的判断,难度不大,易错题是D,注意能导电的不一定是电解质,如金属;电解质不一定导电,如氯化钠固体.

练习册系列答案
相关题目
可逆反应:N2(g)+3H2(g)?2NH3(g)的正、逆反应速度可用各反应物或生成物浓度变化来表示.下列各关系中能说明反应已经达到化学平衡的是( )
| A、3v正(N2)=v逆(H2) |
| B、v正(N2)=v逆(NH3) |
| C、2v正(H2)=3v正(NH3) |
| D、v正(N2)=3v逆(H2) |
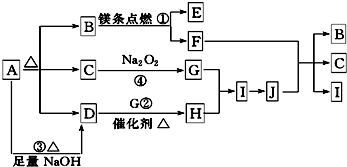
 盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,由如图判断下列关系错误的是( )
盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,由如图判断下列关系错误的是( )| A、A→F,△H=-△H6 |
| B、△H1+△H 2+△H 3+△H 4+△H 5+△H6=1 |
| C、C→F,|△H|=|△H 1+△H 2+△H 6| |
| D、△H1+△H2+△H 3=-△H 4-△H5-△H 6 |
下列各组物质中前者为电解质、后者属于非电解质的是( )
| A、CaO、C2H5OH |
| B、HCl、CH3COOH |
| C、H2S、BaSO4 |
| D、NH3?H2O、Cu |
钢铁发生电化学腐蚀时,负极发生的反应是( )
| A、2H++2e-═H2 |
| B、2H2O+O2+4e-═4OH- |
| C、Fe-2e-═Fe2+ |
| D、4OH-+4e-═2H2O+O2 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,22.4LCCl4中含有的分子数目为NA |
| B、16.8g铁粉与足量水蒸气完全反应转移电子数为0.9NA |
| C、已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.当该反应放出184.8kJ热量时,形成N-H键数为12NA |
| D、1mol乙烯和丙烯的混合气体中α键数为5NA |