题目内容
16.实验室里要配制490mL 0.2mol/L的硫酸钠溶液.(1)请填写下列空白,并对下列操作步骤进行排序BAEFDGC
A.转移:把得到的溶液冷却后小心地沿着玻璃棒注入500 ml的容量瓶中.
B 计算、称量、溶解:在天平上称出14.2g硫酸钠固体,把它放在烧杯里,用适量的蒸馏水溶解.
C.贴标签、装试剂瓶:将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶.
D.定容:继续向容量瓶中加蒸馏水至液面距刻度线1~2cm,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切.如果不小心加多,应该重新配制
E.洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也转入容量瓶中.
F.振荡:轻轻振荡容量瓶
G.摇匀:将瓶塞塞紧,充分摇匀.
(2)下列情况会使所配溶液浓度偏高的是a、e(填字母).
a.某同学定容时俯时容量瓶刻度线
b.没有进行上述的操作步骤E
c.摇匀后发现液面低于刻度线又加水了
d.进行B操作时将少量液体洒到外面
e.未冷却至室温就进行转移
f.称量样品时把样品放在右盘
g.转移前容量瓶有少量蒸馏水.
分析 (1)根据操作过程是计算、量取、溶解、移液、洗涤、定容、摇匀、装瓶等步骤来排序;
A.由于实验室无490mL容量瓶,故应选用500mL容量瓶,配制出500mL溶液,移液时,用玻璃棒引流;
B.根据质量m=cVM计算所需的硫酸钠的质量;
D.定容时,开始直接将水倒入容量瓶,后改用胶头滴管逐滴加入;不小心加多,需重新配制;
(2)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:(1)根据操作过程是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶等步骤来排序可知:正确的操作顺序是:B A E F D G C,
故答案为:B A E F D G C;
A.由于实验室无490mL容量瓶,故应选用500mL容量瓶,配制出500mL溶液,移液时,用玻璃棒引流,将溶液注入500mL容量瓶,
故答案为:玻璃棒;500mL;容量瓶;
B.所需硫酸钠的质量m=cVM=0.2mol/L×0.5L×142g/mol=14.2g,故答案为:14.2;
D.定容时,开始直接将水倒入容量瓶,后改用胶头滴管逐滴加入,至凹液面与刻度线相切;不小心加多,需重新配制,
故答案为:胶头滴管;重新配制;
(2)a.某同学定容时俯时容量瓶刻度线,则溶液体积偏小,故浓度偏高,故a正确;
b.没有进行上述的操作步骤E,会导致溶质的损失,则浓度偏低,故b错误;
c.摇匀后发现液面低于刻度线是正常的,又加水会导致浓度偏低,故c错误;
d.进行B操作时将少量液体洒到外面,会导致溶质的损失,则浓度偏低,故d错误;
e.未冷却至室温就进行转移,待冷却后溶液体积偏小,浓度偏高,故e正确;
f.称量样品时把样品放在右盘,会导致溶质称量减少,则浓度偏低,故f错误;
g.转移前容量瓶有少量蒸馏水,对实验无影响,故g错误;
故答案为:ae.
点评 本题考查了一定物质的量浓度溶液的配制以及误差分析,难度不大,注意实验的基本操作方法和注意事项.

| A. | 氯化钙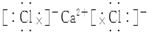 | B. | 硫化钠 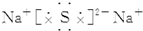 | C. | 氟化钾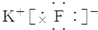 | D. | 过氧化钠 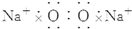 |
| A. | 铁单质 | B. | +2价铁元素 | C. | +3价铁元素 | D. | 三氧化二铁 |
| A. | HCl的结构式为:H-Cl | B. | 水分子的结构式为: | ||
| C. | S2-的离子结构示意图为: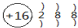 | D. | N2的电子式为: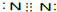 |
| A. | 蒸发皿 | B. | 锥形瓶 | C. | 坩埚 | D. | 容量瓶 |
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+H2O=2AlO2-+3H2↑.
(3)实验室溶解该熔融物,下列试剂中最适宜的试剂是B
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液.
| A. | 硝酸钾 | B. | 硫黄 | C. | 木炭 | D. | 氯化钠 |
| A. | NH4HCO3 | B. | NH4Cl | C. | KClO3 | D. | NaCl |