题目内容
16.能够用来鉴别乙醇、四氯化碳和苯的最简单物质或操作是( )| A. | 钠 | B. | 氢氧化钠溶液 | C. | 水 | D. | 点燃 |
分析 乙醇易溶于水,苯、四氯化碳都不溶于水,但苯的密度比水小,四氯化碳的密度比水大,鉴别时注意考虑实验的安全性以及可行性,以此解答该题.
解答 解:A.加入钠,只与乙醇反应,但钠、乙醇、苯都易燃烧,实验具有不安全性,但由于钠的密度比苯大,比四氯化碳小,可鉴别;
B.加入氢氧化钠溶液,都不反应,可乙醇易溶于水,苯的密度比水小,四氯化碳的密度比水大,可鉴别;
C.乙醇易溶于水,苯、四氯化碳都不溶于水,但苯的密度比水小,四氯化碳的密度比水大,可用水鉴别;
D.点燃时乙醇、苯的燃烧颜色不同,可鉴别,
综上所述,最简单的物质为水,故选C.
点评 本题考查有机物的鉴别,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意鉴别三种物质时,不能仅仅考虑实验现象,还要考虑实验的可行性等因素.

练习册系列答案
相关题目
6.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 2L 1mol/L Na2SO4溶液中离子总数为3NA | |
| B. | 25℃、101.3kPa时,11.2L H2中含有的原子数为NA | |
| C. | 4℃、101.3kPa时,54mL H2O中含有的原子数为3NA | |
| D. | 78g Na2O2与足量水充分反应时电子转移数为NA |
7.有原子序数依次增大的A、B、C、D、E五种短周期元素,它们可两两组成甲、乙、丙、丁四种化合物,各化合物中原子个数比关系如下表:
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多两个;在周期表中,C是E的邻族元素,化学性质活泼;D和E位于同一周期,且D和E的原子序数之和为30.
(1)甲的电子式 ,丁的结构式
,丁的结构式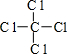
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为 .
.
(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | A:C=1:1 | B:C=1:2 | D:E=1:3 | B:E=1:4 |
(1)甲的电子式
 ,丁的结构式
,丁的结构式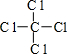
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为
 .
.(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
4.从1L1mol/L的氯化钾溶液中取出50mL溶液,该50mL氯化钾溶液的物质的量浓度为( )
| A. | 0.02 mol/L | B. | 0.05 mol/L | C. | 1 mol/L | D. | 2mol/L |
11.在四个不同的容器中,在不同的条件下进行合成氨的反应,根据下列在相同时间内测定的结果判断,化学反应速率最大的是( )
| A. | v(H2)=0.2 mol/(L•min) | B. | v(N2)=0.2 mol/(L•s) | ||
| C. | v(N2)=0.02 mol/(L•s) | D. | v(H2)=0.04 mol/(L•s) |
8.下列说法正确的是( )
| A. | 煤中含有苯、甲苯、二甲苯等混合物,通过煤的干馏即可得到这些物质 | |
| B. | 煤燃烧时,会产生大量的二氧化硫、氮氧化物、碳氧化物和烟尘等污染物 | |
| C. | 煤是以单质碳为主的复杂混合物 | |
| D. | 把煤高温加强热就是煤的干馏 |
10.下列说法错误的是( )
| A. | 在熔化状态下能导电的化合物一定是离子晶体 | |
| B. | 分子晶体的状态变化只需克服分子间作用力 | |
| C. | 金属键的本质是金属离子与自由电子间的相互作用 | |
| D. | 原子晶体中只存在非极性共价键 |