题目内容
下列实验操作不正确的是( )
| A、用浓硫酸配制一定浓度的稀硫酸时,用量筒量取浓硫酸倒入盛水的烧杯中稀释,且用水洗涤量筒,洗涤液一并注入烧杯 |
| B、除去Fe(OH)3胶体中混有的Cl-离子,可用渗析的方法 |
| C、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出 |
| D、NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
考点:化学实验方案的评价
专题:实验评价题,化学实验基本操作
分析:A.量筒不能洗涤;
B.胶体不能透过半透膜;
C.分液时,上层液体从上口倒出,下层液体从下口流出;
D.蒸发时不能直接将固体蒸干.
B.胶体不能透过半透膜;
C.分液时,上层液体从上口倒出,下层液体从下口流出;
D.蒸发时不能直接将固体蒸干.
解答:
解:A.量筒内壁液体不能用蒸馏水冲洗,否则对导致误差偏大,故A错误;
B.胶体不能透过半透膜,可用渗析的方法分离,故B正确;
C.苯的密度比水小,在溶液上层,应从分液漏斗上口倒出,故C正确;
D.蒸发时不能直接将固体蒸干,防止加热温度过高而导致固体分解而变质,应有晶体析出并剩余少量液体即停止加热,故D正确.
故选A.
B.胶体不能透过半透膜,可用渗析的方法分离,故B正确;
C.苯的密度比水小,在溶液上层,应从分液漏斗上口倒出,故C正确;
D.蒸发时不能直接将固体蒸干,防止加热温度过高而导致固体分解而变质,应有晶体析出并剩余少量液体即停止加热,故D正确.
故选A.
点评:本题考查较为综合,涉及物质的分离、提纯、溶液的配制等知识,为高考常见题型,侧重于学生的分析能力、实验能力和评价能力的考查,注意把握物质的性质的异同以及实验操作的严密性、可行性的评价,难度中等.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,17g羟基中含有的电子数目为10NA |
| B、常温常压下,28g由C2H4和C3H6组成的混合气体中含有的碳原子数目为2NA |
| C、0.05mol熔融的NaHSO4中含有的离子数目为0.15NA |
| D、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
下列叙述正确的是( )
| A、溶液和胶体的本质区别是有无丁达尔效应 |
| B、明矾在水中能形成Al(OH)3胶体,可作净水剂 |
| C、玻璃、水泥和光导纤维的主要成分都是硅酸盐 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色,将SO2通入溴水,溴水褪色后加热也恢复原色 |
1mol某烃完全燃烧可得到2mol CO2;在一定条件下,1mol该烃能与2mol H2发生加成反应,这种烃是( )
| A、CH4 |
| B、C2H4 |
| C、C2H2 |
| D、C3H4 |
常温下,将0.4mol/L的某一元酸HA溶液与0.2mol/L的NaOH溶液等体积混合后(忽略混合前后溶液体积变化),则混合后溶液中的下列关系正确的是( )
| A、可能有c(Na+)>c(A-)>c(HA)>c(OH-)>c(H+) | ||
| B、必定有 c(HA)>c(Na+) | ||
C、可能有c(OH-)=c(H+)+
| ||
| D、c(HA)可能大于0.2mol/L |
含有下列官能团之一的有机物一定会产生银镜反应,此官能团是( )
| A、-OH | B、-CH=CH- |
| C、-CHO | D、-COOH |
 α-AgI是一种固体导体,导电率很高.为研究α-AgI到底是Ag+导电还是I-导电,设计了如图所示实验.下列有关说法不正确的是( )
α-AgI是一种固体导体,导电率很高.为研究α-AgI到底是Ag+导电还是I-导电,设计了如图所示实验.下列有关说法不正确的是( )| A、阳极反应:Ag-e-═Ag+ |
| B、阴极质量不断增大 |
| C、若α-AgI是Ag+导电,则通电一段时间后晶体质量不变 |
| D、若α-AgI是Ag+导电,则通电一段时间后晶体质量减小 |
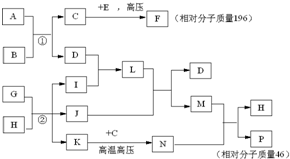 已知C、I、J是常见的气体,A、D是常见的固态非金属单质,E为常见金属,B可用于生产光导纤维,G、H是海水中的主要物质,N是一种盐.在核磁共振氢谱中P有两种峰,F燃烧产生红棕色烟,1molF在真空中完全分解剩余固体的质量是原来的28.6%.试回答下列问题
已知C、I、J是常见的气体,A、D是常见的固态非金属单质,E为常见金属,B可用于生产光导纤维,G、H是海水中的主要物质,N是一种盐.在核磁共振氢谱中P有两种峰,F燃烧产生红棕色烟,1molF在真空中完全分解剩余固体的质量是原来的28.6%.试回答下列问题 有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对电子,F原子核外电子数是B 与C核外电子数之和,D 是主族元素且与E同周期,E能形成红色或砖红色E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示.请回答下列问题:
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对电子,F原子核外电子数是B 与C核外电子数之和,D 是主族元素且与E同周期,E能形成红色或砖红色E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示.请回答下列问题: