题目内容
17.久置空气中会发生颜色变化,但颜色变化不是由于跟氧气反应引起的是( )| A. | 过氧化钠固体 | B. | 苯酚晶体 | C. | 硫酸亚铁晶体 | D. | 亚硫酸钠固体 |
分析 题中过氧化钠、硫酸亚铁、苯酚都可与空气中氧气或水、二氧化碳反应而导致颜色变化,只有过氧化钠与不与氧气反应,据此进行解答.
解答 解:A.过氧化钠和二氧化碳反应生成碳酸钠和氧气而变色,所以过氧化钠颜色变化不是由于跟氧气反应引起的,故A正确;
B.苯酚晶体易被空气中的氧气氧化,由无色变为浅粉红色,则苯酚晶体颜色变化是由于跟氧气反应引起的,故B错误;
C.硫酸亚铁和氧气反应生成硫酸铁,颜色有由绿色变为淡黄色,所以硫酸亚铁颜色变化是由于跟氧气反应引起的,故C错误;
D.亚硫酸钠和氧气反应生成硫酸钠,且颜色没有发生变化,故D错误;
故选A.
点评 本题考查氧化还原反应的应用,题目难度不大,涉及过氧化钠、硫酸亚铁以及苯酚的性质,为高频考点,注意把握物质的性质,注重相关基础知识的积累.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
7.下列有关元素周期律的叙述中,正确的是( )
| A. | 氧化性强弱:Cl2<S | B. | 金属性强弱:K<Na | ||
| C. | 酸性强弱:H3PO4<H2SO4 | D. | 碱性强弱:NaOH<Mg(OH)2 |
8. 室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示,下列说法正确的是( )
室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示,下列说法正确的是( )
 室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示,下列说法正确的是( )
室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示,下列说法正确的是( )| A. | a点所示溶液中c(Na+)>c(A-)>c(H+)>c(OH-) | |
| B. | a、b两点所示溶液中水的电离程度相同 | |
| C. | pH=7时,c(Na+)=c(A-)+c(HA) | |
| D. | b点所示溶液中c(A-)>c(HA) |
5.下列有关氧化还原反应的说法正确的是( )
| A. | 阳离子只有氧化性,阴离子只有还原性 | |
| B. | 还原剂得电子总数与氧化剂失电子总数相等 | |
| C. | 氧化还原反应中的反应物,不是氧化剂就是还原剂 | |
| D. | 非金属元素的最高价氧化物的水化物不一定都具有强氧化性 |
12.下列叙述正确的是( )
| A. | 0.1mol/L的KHC2O4溶液中:c(K+)+c(H+)=c(HC2O4-)+c(OH-)+2c(C2O42-) | |
| B. | 25℃时,将pH=3的盐酸溶液和pH=11的氨水等体积混合,溶液中离子浓度的关系:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 在0.1 mol/LNH4Cl溶液中:c(H+)=c(NH3•H2O)+c(OH-) | |
| D. | 氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c (HClO)] |
2.某原电池的总反应为:2FeCl3+Fe→3FeCl2,则以下叙述正确的是( )
| A. | 铁作阳极 | B. | 炭棒作阴极 | ||
| C. | 正极反应式为Fe3++e-→Fe2+ | D. | 负极反应式为Fe2+-e-→Fe3+ |
9.用下列实验装置进行相应实验,能达到实验目的是( )
| A. |  配制一定物质的量浓度的稀硫酸 | B. | 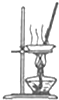 蒸发NH4Cl饱和溶液制备NH4Cl晶体 | ||
| C. | 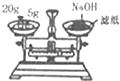 称量NaOH固体 | D. | 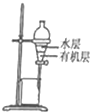 萃取后有机层从下口排放 |