题目内容
200℃时,11.6g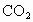 和水蒸气的混合气体与足量的
和水蒸气的混合气体与足量的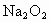 充分反应后,固体质量增加了3.6g,则原混合气体的平均摩尔质量为
充分反应后,固体质量增加了3.6g,则原混合气体的平均摩尔质量为
[ ]
A.11.6g/mol
B.21.6g/mol
C.23.2g/mol
D.36.6g/mol
答案:C
解析:
提示:
解析:
|
由反应式①②可以看出关系式 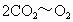 , ,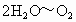 ,即无论 ,即无论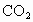 与 与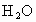 以何比例混合,它们的物质的量等于 以何比例混合,它们的物质的量等于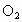 物质的量的2倍。而该反应中产生 物质的量的2倍。而该反应中产生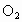 的质量为:11.6g-3.6g=8g, 的质量为:11.6g-3.6g=8g,
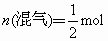 , ,
规律总结: 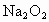 与 与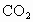 、 、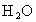 反应存在如下几种关系:①质量关系: 反应存在如下几种关系:①质量关系: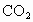 通过足量 通过足量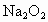 ,被固体吸收的质量相当于“CO”, ,被固体吸收的质量相当于“CO”,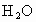 通过足量 通过足量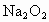 ,被固体吸收的质量相当于“ ,被固体吸收的质量相当于“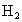 ”。 ”。
②相同条件下(水为气态)体积关系: 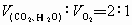 。 。
③物质的量关系: 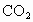 、 、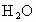 或两者混合物与足量 或两者混合物与足量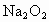 反应时,反应物的物质的量之比为1︰1。 反应时,反应物的物质的量之比为1︰1。
④电子转移关系: 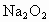 与 与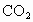 、 、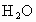 反应时,每生成1mol 反应时,每生成1mol 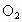 转移2mol 转移2mol 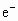 。 。
⑤先后关系,一定量的 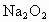 与一定量的 与一定量的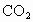 、 、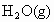 混合物反应时,可视作 混合物反应时,可视作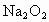 先与 先与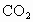 反应,待 反应,待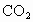 反应完全后, 反应完全后,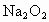 再与 再与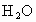 发生反应。 发生反应。
⑥凡可写成 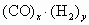 形式的反应物,与 形式的反应物,与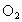 充分反应后再通过足量的 充分反应后再通过足量的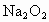 固体时,都可以完全被吸收,固体增加的质量等于反应物的质量(如 固体时,都可以完全被吸收,固体增加的质量等于反应物的质量(如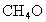 、 、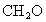 )。 )。 |
提示:
|
题眼点拨:混合气体中未被吸收的是部分氧元素(转变为  )的质量,运用守恒定律可求出答案。 )的质量,运用守恒定律可求出答案。 |

练习册系列答案
相关题目
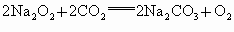
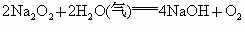
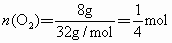
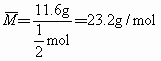
 、
、 、
、 、
、 等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是
( )
等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是
( )