题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4 L重氢(D2)气体分子中含有2NA个中子 |
| B、常温常压下,3.36 L氯气与2.7 g铝充分反应,转移电子数为0.3NA |
| C、Cu-Zn-CuSO4原电池工作时若析出0.1 mol Cu时转移电子数为0.2NA,正极溶解Zn 6.5 g |
| D、1 mol异丁烷中,含共价键数目为10NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量,质子数+中子数=质量数计算;
B、依据标准状况气体摩尔体积为22.4L/mol;
C、依据原电池电极名称和电极反应分析判断;
D、依据异丁烷为烷烃,结合烷烃结构分析计算共价键.
| V |
| Vm |
B、依据标准状况气体摩尔体积为22.4L/mol;
C、依据原电池电极名称和电极反应分析判断;
D、依据异丁烷为烷烃,结合烷烃结构分析计算共价键.
解答:
解:A、依据n=
计算物质的量=
=1mol,质子数+中子数=质量数计算中子=1mol×2×NA=2NA个,故A正确;
B、依据标准状况气体摩尔体积为22.4L/mol,3.36 L氯气物质的量不是0.15mol,故B错误;
C、依据原电池电极反应和电子守恒计算分析判断,析出0.1 mol Cu时转移电子数为0.2NA,负极溶解Zn 6.5 g,故C错误;
D、依据异丁烷为烷烃,结合烷烃结构分析计算1 mol异丁烷中,含共价键数目=1mol×(4-1+10)×NA=13NA,故D错误;
故选A.
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
B、依据标准状况气体摩尔体积为22.4L/mol,3.36 L氯气物质的量不是0.15mol,故B错误;
C、依据原电池电极反应和电子守恒计算分析判断,析出0.1 mol Cu时转移电子数为0.2NA,负极溶解Zn 6.5 g,故C错误;
D、依据异丁烷为烷烃,结合烷烃结构分析计算1 mol异丁烷中,含共价键数目=1mol×(4-1+10)×NA=13NA,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析应用,原电池原理和电极判断,有机物结构理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、聚氯乙烯常用做食品包装材料 |
| B、CO2和CH4都是温室效应气体 |
| C、用乙烷和乙烯分别与氯化氢反应都可得到氯乙烷 |
| D、苯和溴水既能发生取代反应又能发生加成反应 |
下列有机反应中不可能产生两种或两种以上有机产物的是( )
| A、CH3CH═CH2与HCl加成 |
| B、CH3CH2CH2Cl在碱性溶液中水解 |
| C、CH3CH2OH与浓H2SO4混合加热 |
| D、CH3CHBrCH2CH3与NaOH的醇溶液共热 |
科学家们发现有3种氢原子,氕、氘、氚这3种氢原子中质子、中子和电子的数量关系如图所示:

则下列说法不正确的是( )

则下列说法不正确的是( )
| A、H、D、T原子中质子数相同,核外电子数也相同 |
| B、H、D、T原子属于三种不同核素 |
| C、H、D、T原子互为同位素 |
| D、元素的原子都是由质子、中子、电子构成的 |
扑热息痛是一种优良的解热镇痛剂其结构为 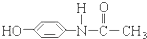 它可能具有的化学性质是( )
它可能具有的化学性质是( )
 它可能具有的化学性质是( )
它可能具有的化学性质是( )| A、不与烧碱溶液反应 |
| B、能与溴水发生取代反应 |
| C、不能被氧化 |
| D、遇FeCl3溶液发生显色反应 |
下列关于物质的量的叙述中,错误的是( )
| A、1 mol任何物质都含有约6.02×1023个原子 |
| B、0.012 kg 12C中含有约6.02×1023个碳原子 |
| C、1 mol水中含有2 molH和1 molO |
| D、1 mol Ne含有6.02×1024个电子 |
下列对聚丙烯的描述有错误的是( )
| A、聚丙烯的分子长链是由C-C键连接而成的 |
| B、聚丙烯分子的长链上有支链 |
| C、聚丙烯每个链节内含3个碳原子 |
| D、聚丙烯能使溴水褪色 |
可逆反应A(g)+3B(g)?2C(g)+D(g) 在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
| A、VD=0.01 mol?(L?s)-1 |
| B、VB=0.6 mol?(L?min)-1 |
| C、VC=0.4 mol?(L?min)-1 |
| D、VA=0.15mol?(L?min)-1 |