题目内容
18.可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,在达到平衡时,要使NH3的浓度达到最大值,最适宜的条件是( )| A. | 低温高压 | B. | 低温低压 | C. | 高温高压 | D. | 使用合适催化剂 |
分析 由N2(g)+3H2(g)?2NH3(g)△H<0可知,为气体体积减小、放热的反应,达到平衡时,要使NH3的浓度达到最大值,应使平衡正向移动,以此来解答.
解答 解:由N2(g)+3H2(g)?2NH3(g)△H<0可知,为气体体积减小、放热的反应,达到平衡时,要使NH3的浓度达到最大值,应使平衡正向移动,则选择高压平衡正向移动,选择降低温度平衡正向移动,而催化剂对平衡移动无影响,
故选A.
点评 本题考查化学平衡的影响因素,为高频考点,把握反应的特点、温度和压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意催化剂不影响平衡移动,题目难度不大.

练习册系列答案
相关题目
7.氢气是人类理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是( )
| A. | 2H2+O2═2H2O△H=-142.9 kJ/mol | B. | 2H2(g)+O2(g)═2H2O(l)△H=-142.9 kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | D. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6 kJ/mol |
13.迄今为止合成的最重的元素是112号元素,它是用${\;}_{30}^{70}$Zn高能原子轰击${\;}_{82}^{208}$Pb的靶子,使锌核与铅核熔合而得,每生成一个112号元素的原子(${\;}_{112}^{277}$R)的同时向外释放出一个中子.下列说法错误的是( )
| A. | 112号元素是金属元素 | |
| B. | 112号元素位于第七周期,是主族元素 | |
| C. | ${\;}_{112}^{277}$R原子中子数为165 | |
| D. | 112号元素为放射性元素 |
3.已知a、b两种脂肪烃的结构简式如图所示.下列说法中不正确的是( )
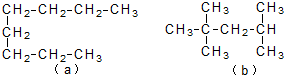
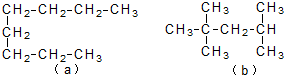
| A. | a和b都不能使酸性KMnO4溶液褪色 | |
| B. | a和b分子中的所有碳碳单键间的键角都相同 | |
| C. | a的沸点比b高 | |
| D. | b脱氢可以形成3种单烯烃分子 |
10.某溶液中含有HCO3-、SO32-、K+、Na+ 四种离子,若向其中加少量Na2O2固体后,溶液中上述离子浓度基本保持不变的是( )
| A. | Na+ | B. | K+ | C. | SO32- | D. | HCO3- |
 请完成下列各题
请完成下列各题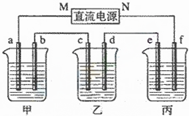 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.85%的NaCl溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.85%的NaCl溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极. ,反应类型取代反应.
,反应类型取代反应.