题目内容
下列水解反应的离子方程式书写正确的是( )
| A、CO32-+2H2O?H2CO3+2OH- |
| B、NH4++H2O?NH3?H2O+H+ |
| C、Al3++3H2O?Al(OH)3↓+H2O |
| D、HCO3-+H2O?H3O++CO32- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.水解分步进行,以第一步为主;
B.水解生成一水合氨、氢离子;
C.水解不能生成沉淀;
D.水解生成碳酸和氢氧根离子.
B.水解生成一水合氨、氢离子;
C.水解不能生成沉淀;
D.水解生成碳酸和氢氧根离子.
解答:
解:A.水解离子反应为CO32-+H2O?HCO3-+OH-,故A错误;
B.铵根离子水解离子反应为NH4++H2O?NH3?H2O+H+,故B正确;
C.水解离子反应为Al3++3H2O?Al(OH)3+3H+,故C错误;
D.水解离子反应为HCO3-+H2O?H2CO3+OH-,故D错误;
故选B.
B.铵根离子水解离子反应为NH4++H2O?NH3?H2O+H+,故B正确;
C.水解离子反应为Al3++3H2O?Al(OH)3+3H+,故C错误;
D.水解离子反应为HCO3-+H2O?H2CO3+OH-,故D错误;
故选B.
点评:本题考查离子反应书写的正误判断,为高频考点,把握盐类水解的规律及多元弱碱离子的水解为解答的关键,侧重水解的离子反应考查,题目难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的措施是( )
| A、向纯水中投入一小块金属钠 |
| B、将水加热煮沸 |
| C、向水中加入Na2CO3 |
| D、向水中加入NH4Cl |
铝硅合金在凝固时收缩率很小,因此这种合金适合铸造,现有下列三种晶体①铝 ②硅③铝硅合金,它们的熔点从低到高的顺序为( )
| A、①<②<③ |
| B、②<①<③ |
| C、①<③<② |
| D、③<①<② |
如图是某同学从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的( ) 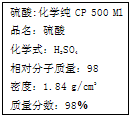

| A、该硫酸的物质的量浓度为9.2 mol/L |
| B、12gC与足量该硫酸共热反应,生成标准状况下气体体积为44.8L |
| C、1 mol Fe与足量的该硫酸反应产生2 g氢气 |
| D、配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
某溶液中大量存在以下浓度的离子:0.2mol/LCl-、0.4mol/LSO42-、0.1mol/LAl3+、0.3mol/LH+、M,则M及其物质的量浓度可能为( )
| A、Na+0.2mol/L |
| B、Zn2+0.2mol/L |
| C、CO32- 0.2mol/L |
| D、Ca2+0.1mol/L |
下列离子方程式中,正确的是( )
| A、铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
| B、大理石溶于醋酸的反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
| C、向稀硫酸溶液中加入铁粉:2Fe+6H+═2Fe3++3H2↑ |
| D、稀硫酸跟氢氧化钡溶液混合:H++OH-═H2O |
下列对溶液、胶体和浊液的认识正确的是( )
| A、三种分散系的分散质均能通过滤纸 |
| B、胶体在一定的条件下也能稳定存在 |
| C、溶液和胶体通常都是无色透明的液体,而浊液不透明 |
| D、胶体区别于其他分散系的本质特征是产生丁达尔现象 |
