��Ŀ����
12��Ԫ��X��Y��Z��M��Q��Ϊ����������Ԫ�أ���ԭ����������������֪Ԫ��Y����������Ӧˮ���������⻯�ﷴӦ������һ���Σ�Zԭ������������������������֮��Ϊ3��4��M����Z�γ����������Ӹ�����Ϊ1��2���ֻ����Qԭ����������������������֮��Ϊ3��4��YX3������Ϊ���壮��1��������A��B��X��Z��M��Q����Ԫ�����������ǿ����ʣ�����������ˮ��Һ�������ͬ�����Ԫ��ԭ����Ŀ֮�Ⱦ�Ϊ1��1��1����A������ˮ���룬B�ܴٽ�ˮ���룬����A��ѧʽΪNaOH��B��ѧʽ��NaHS��
��2��X��Z��X��Q�����γ�18���ӷ��Ӽ��ң�д���ס������ַ�����ˮ��Һ�з�Ӧ����Q���ʻ�ѧ����ʽH2O2+H2S=S+2H2O��X��YҲ���γ�18���ӷ��ӱ�����ͨ����һ��Һ̬���ȼ�ϣ�25�桢��ѹ�£�3.2g������������ȫȼ�շų�����Ϊ62.4kJ����д������ȫȼ���Ȼ�ѧ��Ӧ����ʽN2H4��l��+O2��g��=N2��g��+2H2O��l����H=-624kJ/mol��
��3��X��Y����Ԫ���γ����ӻ��������ʽΪ
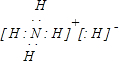 ��
��
���� X��Y��Z��M��Q��Ϊ����������Ԫ�أ���ԭ��������������Ԫ��Y����������Ӧˮ�����������⻯�ﷴӦ������һ���Σ���Y��NԪ�أ�Zԭ������������������������֮��Ϊ3��4����Z��OԪ�أ�M����Z�γ����������Ӹ�����Ϊ1��2�����ֻ������M���ڵ�IA��Ԫ�أ���M��ԭ����������Z������M��NaԪ�أ�Qԭ�ӵ���������������������֮��Ϊ3��4����Q��ԭ����������M������Q��SԪ�أ�YX3������Ϊ���壬��X��HԪ�أ��ݴ˽��
��� �⣺X��Y��Z��M��Q��Ϊ����������Ԫ�أ���ԭ��������������Ԫ��Y����������Ӧˮ�����������⻯�ﷴӦ������һ���Σ���Y��NԪ�أ�Zԭ������������������������֮��Ϊ3��4����Z��OԪ�أ�M����Z�γ����������Ӹ�����Ϊ1��2�����ֻ������M���ڵ�IA��Ԫ�أ���M��ԭ����������Z������M��NaԪ�أ�Qԭ�ӵ���������������������֮��Ϊ3��4����Q��ԭ����������M������Q��SԪ�أ�YX3������Ϊ���壬��X��HԪ�أ�
��1��������A��B��X��Z��M��Q����Ԫ���е�������ɵ�ǿ����ʣ�˵���γɵĻ�������ǿ����Σ�����������ˮ��Һ���������ͬ�����Ԫ�ص�ԭ����Ŀ֮�Ⱦ�Ϊ1��1��1����A������ˮ�ĵ��룬˵��A�ǼB�ܴٽ�ˮ�ĵ��룬˵��B�Ǻ����������ӵ��Σ�����A��NaOH��B��NaHS���ʴ�Ϊ��NaOH��NaHS��
��2��X��Z��X��Q�����γ�18���ӷ��Ӽ��ң���ס��ҷֱ���H2O2 ��H2S��˫��ˮ�����������������ʣ�ͬʱ����ˮ����Ӧ����ʽΪ��H2O2+H2S=S+2H2O��
X��YҲ���γ�18���ӷ��ӱ����仯ѧʽΪ��N2H4����ͨ����һ��Һ̬���ȼ�ϣ�25�桢��ѹ�£�3.2g������������ȫȼ�շų�����Ϊ62.4kJ����1mol��ȼ�շų���������62.4kJ��$\frac{1mol��32g/mol}{3.2g}$=624kJ�����Ա���ȫȼ�յ��Ȼ�ѧ��Ӧ����ʽ��N2H4��l��+O2��g��=N2��g��+2H2O��l����H=-624kJ/mol��
�ʴ�Ϊ��H2O2+H2S=S+2H2O��N2H4��l��+O2��g��=N2��g��+2H2O��l����H=-624kJ/mol��
��3��X��Y����Ԫ���γɵ����ӻ��������⻯泥��⻯淋ĵ���ʽΪ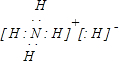 ���ʴ�Ϊ��
���ʴ�Ϊ��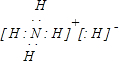 ��
��
���� ���⿼��ṹ����λ�ù�ϵ�ۺ�Ӧ�ã���ȷ�ƶ�Ԫ���ǽⱾ��ؼ���ע���⻯淋���ʽ����д��ʽ��Ϊ�״��㣮

| A�� | 0.1mol•L-1��ˮ�У�c��OH-����c��NH4+�� | |
| B�� | 10mL 0.02mol•L-1HCl��Һ��10mL 0.02mol•L-1Ba��OH��2��Һ��ֻ�ϣ�c��Cl-����c��Ba2+����c��OH-��=c��H+�� | |
| C�� | ��0.1mol•L-1CH3COONa��0.1mol•L-1NH4Cl�������Ϻ����Һ�У�c��H+��+c��CH3COOH����c��NH3•H2O��+c��OH-�� | |
| D�� | 0.1mol•L-1ij��Ԫ�������NaHA��Һ�У�c��H+��+c��H2A���Tc��A2-��+c��OH-�� |
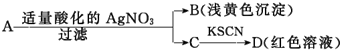
�ɴ˵ó��Ľ����У�����ȷ���ǣ�������
| A�� | Aһ����FeBr3 | B�� | BΪAgBr | ||
| C�� | ��ҺC����Fe3+ | D�� | D��Һ�д���Fe��SCN��3 |
| A�� | NaClO��Һ��Ư��ԭ����SO2��ͬ | |
| B�� | 1 mol Cl2������NaOH��Һ��Ӧת��2 mol���� | |
| C�� | NaClO��Һ������ԭ������ǿ������ʹ�����ʱ��� | |
| D�� | ��84������Һ�롰����顱�����ᣩ��ͬʹ�ÿɴﵽ�������������˫��Ч�� |
| A�� | CO2 | B�� | CH3COOH | C�� | C2H5OH | D�� | Fe |
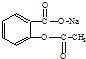 ת��Ϊ
ת��Ϊ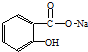 �ķ�����ȷ���ǣ�������
�ķ�����ȷ���ǣ�������| A�� | ��������NaOH��Һ���Ⱥ���ͨ��������CO2 | |
| B�� | ��ϡH2SO4���Ⱥ���������Na2CO3 | |
| C�� | ��������NaOH��Һ���Ⱥ���������ϡH2SO4 | |
| D�� | ��ϡH2SO4���Ⱥ���������NaOH |
| Ԫ�ط��� | X | Y | Z | R | T |
| ԭ�Ӱ뾶��nm�� | 0.160 | 0.089 | 0.102 | 0.143 | 0.074 |
| ��Ҫ���ϼ� | +2 | +2 | -2��+4��+6 | +3 | -2 |
| A�� | ������ϡ���ᷴӦ�����ʿ�����R��Y��X | |
| B�� | ���Ӱ뾶��X2+��T2- | |
| C�� | Ԫ������������Ӧ��ˮ����ļ��ԣ�R��X | |
| D�� | ��ͬ�����£������ʵ����ĵ������������Ϸų������Ķ��٣�T��Z |
| A�� | Mg�Ļ��ϼ���0���ߵ�+2������MgO�ǻ�ԭ���� | |
| B�� | �ɴ˷�Ӧ�����ж�������CO2��MgO����ԭ��Mg��C | |
| C�� | CO2�������������ֳ������ԣ�����������Ӧ | |
| D�� | Mgԭ��ʧȥ�ĵ�����Ŀ������ԭ�ӵõ��ĵ�����Ŀ |
| A�� | ��ʹ����KMnO4��Һ��ɫ | B�� | ������ϩͨ���ӳɷ�Ӧ��ȡ | ||
| C�� | ����ȩ��Ϊͬ���칹�� | D�� | ͨ��ȡ����Ӧ����ȡ������ |