题目内容
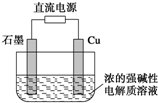 Cu2O是一种半导体材料,基于绿色化学理论设计的制取Cu2O的电解池示意图如图,电解总反应为2Cu+H2O
Cu2O是一种半导体材料,基于绿色化学理论设计的制取Cu2O的电解池示意图如图,电解总反应为2Cu+H2O
| ||
| A、石墨电极上产生氢气 |
| B、铜电极发生还原反应 |
| C、铜电极接直流电源的负极 |
| D、当有0.1 mol电子转移时,有0.1 mol Cu2O生成 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据电解总反应为2Cu+H2O
Cu2O+H2↑,可以知道金属铜为阳极材料,在阳极发生失电子的氧化反应,在阴极上是氢离子发生得电子的还原反应,根据电极方程式结合电子守恒计算生成的Cu2O.
| ||
解答:
解:A、电解总反应:2Cu+H2O
Cu2O+H2↑,金属铜失电子,说明金属铜一定作阳极,石墨做阴极,在阴极上是溶液中的氢离子得电子,产生氢气,故A正确;
B、铜电极本身失电子,发生氧化反应,故B错误;
C、铜电极是电解池的阳极,接直流电源的正极,故C错误;
D、反应2Cu+H2O═Cu2O+H2↑失电子的量为2mol,生成氧化亚铜1mol,所以当有0.1mol电子转移时,有0.05molCu2O,故D错误.
故选A.
| ||
B、铜电极本身失电子,发生氧化反应,故B错误;
C、铜电极是电解池的阳极,接直流电源的正极,故C错误;
D、反应2Cu+H2O═Cu2O+H2↑失电子的量为2mol,生成氧化亚铜1mol,所以当有0.1mol电子转移时,有0.05molCu2O,故D错误.
故选A.
点评:本题考查学生电解池的工作原理,注意阴阳极的判断及电极反应式的书写,要求学生熟记教材知识,并会灵活运用,题目难度不大.

练习册系列答案
相关题目
1mol Na2O2与2mol NaHCO3固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
| A、Na2CO3 |
| B、Na2O2、Na2CO3 |
| C、NaOH、Na2CO3 |
| D、Na2O2、NaOH、Na2CO3 |
 烧杯A中盛放0.1mol?L-1的H2SO4溶液,烧杯B中盛放0.1mol?L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法正确的是( )
烧杯A中盛放0.1mol?L-1的H2SO4溶液,烧杯B中盛放0.1mol?L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法正确的是( )| A、A为电解池,B为原电池 |
| B、Fe电极发生还原反应 |
| C、当A烧杯中产生0.1 mol气体,B烧杯中产生气体也为0.1mol |
| D、一段时间后,B烧杯中溶液的浓度增大 |
Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”.”.S2O32-和Cl2反应的产物之一为SO42-下列说法不正确的是( )
| A、该反应中还原剂是S2O32- |
| B、H2O参与该反应,且作氧化剂 |
| C、根据该反应可判断氧化性:Cl2>SO42- |
| D、上述反应中,每生成1 molSO42-,可脱去2 mol Cl2 |