题目内容
NaNO2是一种食品添加剂,它能致癌。酸性高锰酸钾溶液与亚硝酸钠的反应方程式是:
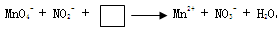 。下列叙述中正确的是
。下列叙述中正确的是
A.该反应中NO2-被还原
B.反应过程中溶液的pH变小
C.生成1molNaNO3需要消耗0.4molKMnO4
D.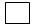 中的粒子是OH-
中的粒子是OH-
C
【解析】
试题分析:A、根据题给反应分析,NO2-中氮元素的化合价从+3价升高到+5价,失去2个电子,被氧化,错误;C、Mn元素的化合价从+7价降低到+2价,得到5个电子,根据电子的得失守恒可知,氧化剂和还原剂的物质的量之比是2︰5,生成1molNaNO3需要消耗0.4molKMnO4,正确;配平该反应方程式为:2MnO4- +5NO2- +6H+ 2Mn2+ + 5NO3- + 3H2O,B和D错误。
2Mn2+ + 5NO3- + 3H2O,B和D错误。
考点:考查氧化还原反应的有关计算和判断

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示,取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是
阴离子 | OH-、NO | 阳离子 | NH |
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④ C.③⑤ D.①⑤
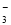 、SO
、SO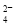
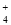 、Na+、Mg2+
、Na+、Mg2+