题目内容
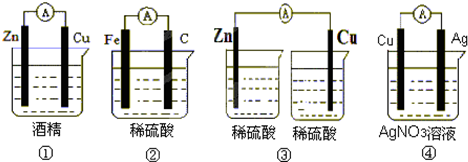
下列各情况,在其中Fe片腐蚀由快到慢的顺序是


考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:先判断装置是原电池还是电解池,再根据原电池正负极腐蚀的快慢比较,作原电池负极和电解池阳极的金属易被腐蚀,作原电池正极或电解池阴极的金属易被保护,金属腐蚀快慢顺序是:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀.
解答:
解:根据图知,(2)(3)装置是原电池,在(2)中,金属铁做负极,(3)中金属铁作正极,做负极的腐蚀速率快,并且两个电极金属活泼性相差越大,负极金属腐蚀速率越快,正极被保护,并且原电池原理引起的腐蚀>化学腐蚀,所以(2)>(3),
(4)(5)装置是电解池,(4)中金属铁为阴极,(5)中金属铁为阳极,阳极金属被腐蚀速率快,阴极被保护,即(5)>(4),
根据电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀,并且原电池的正极金属腐蚀速率快于电解池的阴极金属腐蚀速率,
所以铁腐蚀快慢顺序为:(5)>(2)>(1)>(3)>(4);
故答案为:(5)>(2)>(1)>(3)>(4).
(4)(5)装置是电解池,(4)中金属铁为阴极,(5)中金属铁为阳极,阳极金属被腐蚀速率快,阴极被保护,即(5)>(4),
根据电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀,并且原电池的正极金属腐蚀速率快于电解池的阴极金属腐蚀速率,
所以铁腐蚀快慢顺序为:(5)>(2)>(1)>(3)>(4);
故答案为:(5)>(2)>(1)>(3)>(4).
点评:本题考查了金属的腐蚀与防护,明确原电池和电解池原理是解本题关键,知道作原电池负极或电解池阳极的金属易被腐蚀,难度不大.

练习册系列答案
相关题目
如图所示,关于该装置的下列叙述中,不正确的是( )
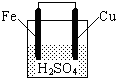

| A、铁棒是负极,发生氧化反应 |
| B、铜棒上有气体放出 |
| C、稀硫酸的pH值不断减小 |
| D、电池总反应方程式可表示为:Fe+2H+=Fe2++H2↑ |
进行化学实验必须注意安全,下列说法正确的是( )
| A、不慎将浓硫酸溶液沾到皮肤上,要立即涂上大量浓碱溶液将其中和 |
| B、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛[ |
| C、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下加入浓硫酸 |
| D、酒精灯着火时可用水扑灭 |
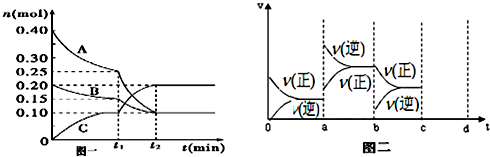
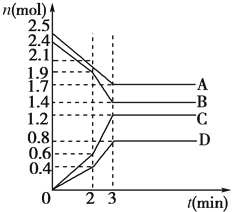 在某一容积为2L的密闭容器中,A、B、C、D四种气体物质的量(n)随时间(t)的变化曲线如图所示:
在某一容积为2L的密闭容器中,A、B、C、D四种气体物质的量(n)随时间(t)的变化曲线如图所示: 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表: