题目内容
10.向一恒容密闭容器中充入1mol N2和3mol H2,在一定条件下反应.下列叙述中,能说明上述反应达到化学平衡状态的是( )| A. | 容器内混合气体的密度不随时间的变化而变化 | |
| B. | 混合气体的总物质的量不随时间的变化而变化 | |
| C. | 混合气体的总质量不随时间的变化而变化 | |
| D. | 单位时间内每消耗3mol H2,同时生成2mol NH3 |
分析 可逆反应N2+3H2?2NH3达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断.
解答 解:A.容器体积不变,气体质量不变,密度始终不变,所以密度不变不能作为反应达到平衡状态的标志,故A错误;
B.反应前后气体物质的量不同,所以气体物质的量不变说明反应达到平衡状态,故B正确;
C.该反应前后都是气体,据质量守恒定律,混合气体的质量始终不变,不能根据混合气体的质量判断平衡状态,故C错误;
D.消耗氢气和生成氨气都是正反应,无论是否平衡,其速率之比等于化学计量数之比,无法判断正逆反应速率相等,故D错误;
故选B.
点评 本题考查化学平衡状态的判断,题目难度不大,明确化学平衡状态的特征为解答关键,A为易错点,只有混合气体的密度始终不变,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
7.向BaCl2溶液中通入SO2气体至饱和,未见沉淀生成,继续通入另-种气体仍无沉淀产生,则通入的气体可能是( )
| A. | NO2 | B. | NH3 | C. | CO2 | D. | Cl2 |
1.在合成氨反应中,下列说法可以确定反应已达到化学平衡状态的是( )
| A. | 当有1molN≡N键断裂的同时,有3molH-H键断裂 | |
| B. | 当有1molN≡N键断裂的同时,有6molN-H键形成 | |
| C. | 当有1molN≡N键断裂的同时,有6molH-H键形成 | |
| D. | 当有1molN≡N键断裂的同时,有6molN-H键断裂 |
18.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解质溶液.下列说法正确的是( )
| A. | 电流方向是由Zn经导线到K2FeO4 | |
| B. | 正极反应式为 2FeO42-+10H++6e-═Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
5.下列过程既有化学键的破坏又有化学键的形成的是( )
| A. | 碘升华 | B. | 冰融化 | C. | 浓盐酸挥发 | D. | NH4Cl受热分解 |
15.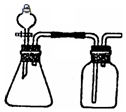 利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )
利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )
①亚硫酸钠和浓硫酸
②铝和烧碱溶液
③铜和稀硝酸
④铜和浓硫酸
⑤双氧水(H2O2)和二氧化锰
⑥铜和浓硝酸.
 利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )
利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )①亚硫酸钠和浓硫酸
②铝和烧碱溶液
③铜和稀硝酸
④铜和浓硫酸
⑤双氧水(H2O2)和二氧化锰
⑥铜和浓硝酸.
| A. | ①⑤⑥ | B. | ①③⑥ | C. | ①②⑤ | D. | ③⑤⑥ |
2.下列有关说法不正确的是( )
| A. | “蚕月条桑…八月载绩”,描述的是采桑与织麻布,鉴别丝绸与棉麻制品可采用灼烧的方法 | |
| B. | 尼龙绳、宣纸、羊绒衫、棉衬衣这些生活用品中都主要由合成纤维制造 | |
| C. | 古代造纸是以树皮、麻头、破布、鱼网等植物纤维为原料,纤维素是天然的高分子材料 | |
| D. | 加热能杀死流感病毒是因为蛋白质受热变性 |
18.下列说法正确的是( )
| A. | 所有共价键都有方向性 | |
| B. | s轨道和p轨道重叠可以形成π键 | |
| C. | 若把H2S分子写成H3S分子,违背了共价键的饱和性 | |
| D. | 两个原子之间形成共价键时,可形成多个σ键 |
 如图电解装置中,电极A是由金属M制成的,B、C和D都是铂电极,甲中的电解质溶液为MSO4,乙中的电解质为H2SO4.E、F是外接直流电源的两极,电路接通后,电极B上有金属M析出.(已知金属M无变价)
如图电解装置中,电极A是由金属M制成的,B、C和D都是铂电极,甲中的电解质溶液为MSO4,乙中的电解质为H2SO4.E、F是外接直流电源的两极,电路接通后,电极B上有金属M析出.(已知金属M无变价)