��Ŀ����
��������ɸ�������ɺ����ʽ��з��ࣺ
��������һ��ԡ�һЩ������ˮ��Ӧ���ķ���ͼ���밴Ҫ����գ�
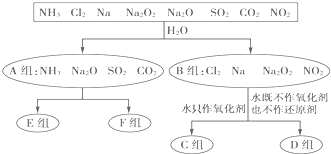
��1�����������У��ֳ�A��B����������� ��
��2��C��������ˮ��Ӧ�����ӷ���ʽΪ ��
��3��D��������ˮ��Ӧ�У��������ͻ�ԭ�����ʵ���֮��Ϊ1��1�������� ���ѧʽ����
����֪���⻯��ͭ��CuH����һ���������ʣ����ȶ����ֽ⣻����ϡ���ᷴӦ���������壻Cu+�������������·�����Ӧ��2Cu+=Cu2++Cu��
����������Ϣ���ش��������⣺
��4��CuH����CuSO4��Һ�͡���һ���ʡ���40��50��ʱ��Ӧ�õ����ڸ÷�Ӧ�С���һ���ʡ��� �������������ԭ��������
��5��CuH�ܽ���ϡ���������ɵ������� ���ѧʽ����
��6�������CuH�ܽ���������ϡ���������ɵ�����ֻ��NO����д��CuH�ܽ�������ϡ�����з�Ӧ�����ӷ���ʽ�� ��
��������һ��ԡ�һЩ������ˮ��Ӧ���ķ���ͼ���밴Ҫ����գ�

��1�����������У��ֳ�A��B�����������
��2��C��������ˮ��Ӧ�����ӷ���ʽΪ
��3��D��������ˮ��Ӧ�У��������ͻ�ԭ�����ʵ���֮��Ϊ1��1��������
����֪���⻯��ͭ��CuH����һ���������ʣ����ȶ����ֽ⣻����ϡ���ᷴӦ���������壻Cu+�������������·�����Ӧ��2Cu+=Cu2++Cu��
����������Ϣ���ش��������⣺
��4��CuH����CuSO4��Һ�͡���һ���ʡ���40��50��ʱ��Ӧ�õ����ڸ÷�Ӧ�С���һ���ʡ���
��5��CuH�ܽ���ϡ���������ɵ�������
��6�������CuH�ܽ���������ϡ���������ɵ�����ֻ��NO����д��CuH�ܽ�������ϡ�����з�Ӧ�����ӷ���ʽ��
���㣺ͭ����������Ҫ���������Ҫ����,������ԭ��Ӧ
ר�⣺
������I����1������A��B������ˮ��Ӧ����ʽ������������
��2��C��������ˮ��Ӧˮֻ����������ֻ���ƣ�
��3��D��������ˮ��Ӧ�У������������ͻ�ԭ�����ʵ���֮��Ϊ1��1��������
��4�����ݻ��ϼ۵ı仯�ж�����������ԭ����
��5��CuH�ܽ���ϡ�����У�CuH�е�H-ʧ���ӣ�������H+�õ��ӣ�
��6��Cu+�����������·����ķ�Ӧ�ǣ�2Cu+=Cu2++Cu��ϡ�������ǿ�����ԣ��ܺ�ͭ��Ӧ����һ���������壮
��2��C��������ˮ��Ӧˮֻ����������ֻ���ƣ�
��3��D��������ˮ��Ӧ�У������������ͻ�ԭ�����ʵ���֮��Ϊ1��1��������
��4�����ݻ��ϼ۵ı仯�ж�����������ԭ����
��5��CuH�ܽ���ϡ�����У�CuH�е�H-ʧ���ӣ�������H+�õ��ӣ�
��6��Cu+�����������·����ķ�Ӧ�ǣ�2Cu+=Cu2++Cu��ϡ�������ǿ�����ԣ��ܺ�ͭ��Ӧ����һ���������壮
���
�⣺I����1��A����ˮ��Ӧ�������ɶ�Ӧ��������B����ˮ��Ӧ��������������ԭ��Ӧ���ʷֳ�A��B�������������ˮ��Ӧ�Ƿ���������ԭ��Ӧ��
�ʴ�Ϊ����ˮ��Ӧ�Ƿ���������ԭ��Ӧ��
��2��C��������ˮ��Ӧˮֻ����������ֻ���ƣ��������ӷ���ʽΪ��2Na+2H2O�T2Na++2OH-+H2�����ʴ�Ϊ��2Na+2H2O�T2Na++2OH-+H2����
��3��D��������ˮ��Ӧ�У�ˮ������������Ҳ������ԭ����ΪCl2��Na2O2�������������ͻ�ԭ�����ʵ���֮��Ϊ1��1Ҳ��Cl2��Na2O2���ʴ�Ϊ��Cl2��Na2O2��
��4���ɻ��ϼ۵ı仯��֪��CuSO4����������������һ��������ԭ�����ʴ�Ϊ����ԭ����
��5��CuH�ܽ���ϡ�����У�����2CuH+2H2SO4=2CuSO4+3H2������������ΪH2���ʴ�Ϊ��H2��
��6��Cu+�����������·����ķ�Ӧ�ǣ�2Cu+=Cu2++Cu��ϡ�������ǿ�����ԣ�CuH���л�ԭ�ԣ����߷�Ӧ����һ���������塢ͭ���ӡ�H2O���������ᷴӦ�����ӷ�ӦΪCuH+3H++NO3-=Cu2++2H2O+NO�����ʴ�Ϊ��CuH+3H++NO3-=Cu2++2H2O+NO����
�ʴ�Ϊ����ˮ��Ӧ�Ƿ���������ԭ��Ӧ��
��2��C��������ˮ��Ӧˮֻ����������ֻ���ƣ��������ӷ���ʽΪ��2Na+2H2O�T2Na++2OH-+H2�����ʴ�Ϊ��2Na+2H2O�T2Na++2OH-+H2����
��3��D��������ˮ��Ӧ�У�ˮ������������Ҳ������ԭ����ΪCl2��Na2O2�������������ͻ�ԭ�����ʵ���֮��Ϊ1��1Ҳ��Cl2��Na2O2���ʴ�Ϊ��Cl2��Na2O2��
��4���ɻ��ϼ۵ı仯��֪��CuSO4����������������һ��������ԭ�����ʴ�Ϊ����ԭ����
��5��CuH�ܽ���ϡ�����У�����2CuH+2H2SO4=2CuSO4+3H2������������ΪH2���ʴ�Ϊ��H2��
��6��Cu+�����������·����ķ�Ӧ�ǣ�2Cu+=Cu2++Cu��ϡ�������ǿ�����ԣ�CuH���л�ԭ�ԣ����߷�Ӧ����һ���������塢ͭ���ӡ�H2O���������ᷴӦ�����ӷ�ӦΪCuH+3H++NO3-=Cu2++2H2O+NO�����ʴ�Ϊ��CuH+3H++NO3-=Cu2++2H2O+NO����
���������⿼�����ʵ����ʼ�������ԭ��Ӧ��Ϊ��Ƶ���㣬�������ʵ����ʡ�ϰ���е���Ϣ�������ķ�ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��������ԭ��Ӧ��Ӧ�ã���Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
���������ϵ�������ǣ�������
| A����NH3��ˮ��Һ���Ե��磬����NH3�ǵ���� |
| B����SO2����ʹ��ˮ��ɫ������SO2����Ư���� |
| C����ij������Һ����ɫ�ʻ�ɫ������������ΪNaOH |
| D����Al����ǿ����Һ��Ӧ����ƫ�����Σ�����Al��һ���ķǽ����� |
������һ����Ч���������Ƽ�������Ч�ط�ֹ����ֲ�ų⣬��ṹ��ʽ��ͼ��ʾ�� ���й�����˵��������ǣ�������
���й�����˵��������ǣ�������
 ���й�����˵��������ǣ�������
���й�����˵��������ǣ�������| A������FeCl3��Һ������ɫ��Ӧ |
| B����һ�������¿ɷ����ӳɡ�ȡ������ȥ��Ӧ |
| C��1 mol�����������4 mol H2��Ӧ |
| D��1 mol�����������3 mol NaOH��Ӧ |
 PM2.5������ο������Ⱦ������ȼú������أ�ȼú��ͬʱ�ŷŴ�����CO2��SO2��NOx
PM2.5������ο������Ⱦ������ȼú������أ�ȼú��ͬʱ�ŷŴ�����CO2��SO2��NOx
 ����U�ܣ���Ӳ�ʲ��������ƣ�������ܡ��ƾ��ơ����ҺͲ������ܵ����������ͼװ����֤ʵϡ������ͭ��Ӧ����NO
����U�ܣ���Ӳ�ʲ��������ƣ�������ܡ��ƾ��ơ����ҺͲ������ܵ����������ͼװ����֤ʵϡ������ͭ��Ӧ����NO
