题目内容
下列实验中,所选装置不合理的是( )


| A、粗盐提纯,选①和② |
| B、用CCl4提取碘水中的碘,选③ |
| C、分离Na2CO3溶液和CH3COOC2H5,选④ |
| D、用NaOH溶液吸收Cl2,选⑤ |
考点:化学实验方案的评价
专题:实验评价题
分析:A.粗盐提纯过程中的操作为:溶解、过滤、蒸发结晶;
B.提取碘水中的碘采用萃取、分液的方法;
C.分离互不相溶的液体采用分液的方法;
D.氯气极易溶于氢氧化钠溶液.
B.提取碘水中的碘采用萃取、分液的方法;
C.分离互不相溶的液体采用分液的方法;
D.氯气极易溶于氢氧化钠溶液.
解答:
解:A.粗盐提纯过程中的操作为:溶解、过滤、蒸发结晶,所以选①和②,故A正确;
B.碘在四氯化碳中的溶解度大于在水中的溶解度,四氯化碳和碘不反应、和水不互溶,所以提取碘水中的碘采用萃取、分液的方法,则选③,故B正确;
C.碳酸钠溶液和乙酸乙酯不互溶,应该采用分液的方法分离,则选③,故C错误;
D.2NaOH+Cl2=NaCl+NaClO+H2O,所以用⑤吸收氯气,故D正确;
故选C.
B.碘在四氯化碳中的溶解度大于在水中的溶解度,四氯化碳和碘不反应、和水不互溶,所以提取碘水中的碘采用萃取、分液的方法,则选③,故B正确;
C.碳酸钠溶液和乙酸乙酯不互溶,应该采用分液的方法分离,则选③,故C错误;
D.2NaOH+Cl2=NaCl+NaClO+H2O,所以用⑤吸收氯气,故D正确;
故选C.
点评:本题考查化学实验评价,涉及混合物的分离和提纯、尾气处理,明确物质的性质即可解答,根据物质的性质采用合适的分离方法进行分离,采用的分离方法有:加热、萃取、过滤、蒸馏、渗析等,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列物质水溶液经加热浓缩、蒸干后适当加热不能得到原物质的是( )
①NH4HCO3; ②CaCl2; ③AlCl3; ④Cu(NO3)2; ⑤FeCl2;⑥K2SO3; ⑦KMnO4; ⑧KAl(SO4)2.
①NH4HCO3; ②CaCl2; ③AlCl3; ④Cu(NO3)2; ⑤FeCl2;⑥K2SO3; ⑦KMnO4; ⑧KAl(SO4)2.
| A、①③④⑤⑥⑦ | B、①②③⑤ |
| C、①③④⑤ | D、以上均不能 |
在集气瓶中使用甲烷与氧气混合,点燃,进行爆炸性试验,下列甲烷与氧气的体积比中爆炸声最大的是( )
| A、1:1 | B、1:2 |
| C、1:3 | D、3:1 |
用下列实验装置进行相应实验,能达到实验目的是( )
A、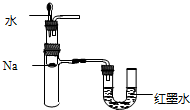 验证Na和水反应放热 |
B、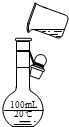 将溶液定容到100mL |
C、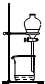 分离酒精和水 |
D、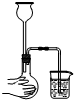 检查装置的气密性 |
下列说法正确的是( )
| A、CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 |
| D、晶体中一定存在化学键 |
加热条件下,将24g CuO、Fe2O3的混合物与充足的CO完全反应,并将反应后的气体全部通入到澄清石灰水中,得到白色沉淀40g.下列有关叙述中正确的是( )
| A、原混合物中CuO与Fe2O3物质的量的比为l:l |
| B、反应后所得CO2的质量为8.8g |
| C、参加反应的CO的质量为8.4g |
| D、原混合物中CuO与Fe2O3的质量比为1:1 |
用下列实验装置进行的实验中,不能达到相应实验目的是( )
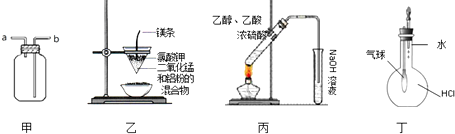

| A、装置甲:气体从a口进入,收集NH3 |
| B、装置乙:可制得金属锰 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:验证HCl气体在水中的溶解性 |
物质的量浓度、体积都相同的一元酸和一元碱恰好中和时,溶液将( )
| A、显酸性 | B、显中性 |
| C、显碱性 | D、无法确定酸碱性 |