题目内容
6.3月22日是世界水日.下列有关水的说法中不正确的是( )| A. | 用太阳能蒸馏海水是海水淡化的方法之一 | |
| B. | 推广使用无磷洗衣粉主要是为了防止水体富营养化 | |
| C. | 水厂常用硫酸亚铁和氯气处理水,可起到消毒杀菌和除去水中悬浮杂质的作用 | |
| D. | 水在3.98℃时,主要以(H2O)2存在,这两个水分子间是以共价键相结合的 |
分析 合理利用水资源,应节约用水,减少污染物的排放,可通过淡化海水获取淡水,水分子间含有氢键,以此解答该题.
解答 解:A.水的沸点较低,蒸馏可得到淡水,故A正确;
B.含磷洗衣粉可导致水体富营养化,应减少使用,故B正确;
C.使用硫酸亚铁和氯气处理水,生成氢氧化铁胶体,可除去水的悬浮物氯气具有杀菌消毒的作用,故C正确;
D.水分子之间存在氢键,故D错误.
故选D.
点评 本题考查水资源的使用,为高频考点,侧重化学与生后、生产的考查,有利于培养学生良好的科学素养,题目难度不大,注意相关基础知识的积累,树立保护环境的意识.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
14.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 乙烯可与KMnO4溶液发生反应 | 乙烯具有还原性 |
| D | 乙醇的沸点比乙酸的沸点高 | 乙醇和乙酸可通过蒸馏初步分离 |
| A. | A | B. | B | C. | C | D. | D |
1.某化学实验室产生的废液中含有Fe3+、Cu2+、Zn2+、Cl-四种离子,现设计下列方案对废液进行处理,以回收金属并制备较纯净的氯化锌、氯化铁晶体.
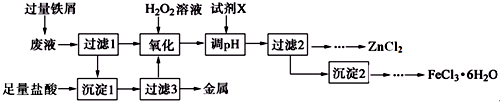
(1)氧化过程中加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,加入H2O2后立即有大量气泡生成,可能的原因是溶液中金属阳离子催化H2O2分解.
(2)Fe3+水解的平衡常数表达式为Kh=$\frac{{c}^{3}({H}^{+})}{c(F{e}^{3+})}$,加入试剂X调pH合适范围为[3.7,5.4),X可以是下列试剂中的AD(填字母).
A.ZnCO3 B.NH3•H2O C.ZnCl2 D.ZnO
(3)由沉淀2获得FeCl3•6H2O晶体的操作为①加入过量盐酸溶解;②蒸发浓缩、冷却结晶;③过滤、洗涤、干燥.

| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 5.2 | 5.4 |
| 完全沉淀pH | 3.7 | 9.6 | 6.9 | 7.8 |
(2)Fe3+水解的平衡常数表达式为Kh=$\frac{{c}^{3}({H}^{+})}{c(F{e}^{3+})}$,加入试剂X调pH合适范围为[3.7,5.4),X可以是下列试剂中的AD(填字母).
A.ZnCO3 B.NH3•H2O C.ZnCl2 D.ZnO
(3)由沉淀2获得FeCl3•6H2O晶体的操作为①加入过量盐酸溶解;②蒸发浓缩、冷却结晶;③过滤、洗涤、干燥.
11.水分子中不存在( )
| A. | 共价键 | B. | 离子键 | C. | 极性键 | D. | 共用电子对 |
18.下列说法正确的是( )
| A. | 室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷 | |
| B. | 用NaOH溶液可以区分HCOOCH3和HCOOCH2CH3 | |
| C. | 用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 | |
| D. | 油脂在酸性或碱性条件下均能发生水解反应,且产物相同 |
15.实验室中不可用于制取NH3的有( )
| A. | 加热浓氨水 | B. | 生石灰和浓氨水 | ||
| C. | Ca(OH)2和NH4Cl共热 | D. | 用氢气和氮气催化合成 |
16.不能将溴水、碘水中的溴、碘萃取出来的溶剂是( )
| A. | 四氯化碳 | B. | 直馏汽油 | C. | 酒精 | D. | 苯 |

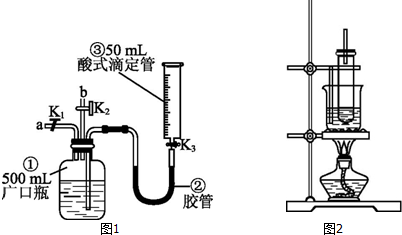
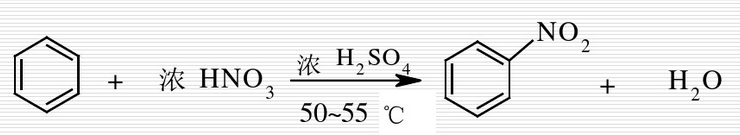 ;
;