题目内容
下列事实,不能用平衡移动原理解释的是( )
| A、硫酸工业中,增大O2的浓度有利于提高SO2的转化率 |
| B、将FeS固体投入到含有Cu2+的废水中以除去Cu2+ |
| C、选择合适的催化剂可使水在较低温度下分解 |
| D、滴有酚酞的CH3COONa溶液,加热后颜色变深 |
考点:化学平衡移动原理
专题:化学平衡专题
分析:平衡移动原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,平衡移动原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用平衡移动原理解释,平衡移动原理对所有的动态平衡都适用.
解答:
解:A.二氧化硫和氧气反应中存在平衡2SO2+O2
2SO3,增大压强浓度平衡向正反应方向移动,所以有利于提高二氧化硫转化率,能用平衡移动原理解释,故A不选;
B.FeS中存在溶解平衡FeS(s)?Fe2++S2-,CuS的溶度积常数小于FeS,将FeS固体投入到含有Cu2+的废水中以除去Cu2+,能将FeS转化为CuS,从而除去铜离子,所以能用平衡移动原理解释,故B不选;
C.催化剂只能改变反应速率不能改变平衡移动,所以不能用平衡移动原理解释,故C选;
D.醋酸钠中存在水解平衡CH3COO-+H2O?CH3COOH+OH-,且盐类水解是吸热反应,升高温度促进水解,滴有酚酞的CH3COONa溶液,加热后颜色变深,所以可以用平衡移动原理解释,故D不选;
故选C.
| 催化剂 |
| △ |
B.FeS中存在溶解平衡FeS(s)?Fe2++S2-,CuS的溶度积常数小于FeS,将FeS固体投入到含有Cu2+的废水中以除去Cu2+,能将FeS转化为CuS,从而除去铜离子,所以能用平衡移动原理解释,故B不选;
C.催化剂只能改变反应速率不能改变平衡移动,所以不能用平衡移动原理解释,故C选;
D.醋酸钠中存在水解平衡CH3COO-+H2O?CH3COOH+OH-,且盐类水解是吸热反应,升高温度促进水解,滴有酚酞的CH3COONa溶液,加热后颜色变深,所以可以用平衡移动原理解释,故D不选;
故选C.
点评:本题考查化学平衡移动原理,化学平衡移动原理适用于所有可逆反应,注意催化剂不能改变平衡移动,只能影响反应速率,易错选项是BC.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
SO2Cl2是一种重要的试剂,可用如下方法制备:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0.下列措施既能加快反应速率又能提高SO2转化率的是( )
| A、升高温度 |
| B、缩小容器体积 |
| C、增大容器体积 |
| D、降低温度 |
下列物质中互为同分异构体的是( )
| A、O2和O3 |
B、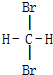 和 和 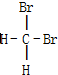 |
| C、CH3COOH和HCOOCH3 |
D、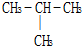 和 和 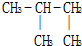 |
工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:对上述流程中的判断正确的是( )
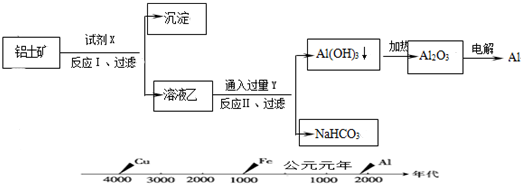

| A、试剂X为稀硫酸 |
| B、反应Ⅱ中生成Al(OH)3的反应为:CO2+2AlO2-+3H2O═2Al(OH)3↓+CO32- |
| C、人类对金属的使用历史与金属活动顺序和冶炼的难易程度有关 |
| D、Al2O3熔点很高,电解耗能大,可采用电解熔融AlCl3冶炼Al |
对于密闭容器中进行的反应:2NO2?N2O4,下列说法正确的是( )
| A、增大NO2的浓度,平衡常数增大 |
| B、增大N2O4的浓度,平衡常数增大 |
| C、增大NO2的浓度,正反应速率加快,逆反应速率减慢 |
| D、增大NO2的浓度,平衡常数不变 |
下列各组离子中,在溶液中能大量共存的是( )
| A、H+,OH-,Na+,SO42- |
| B、Fe3+,Cl-,K+,I- |
| C、Cu2+,NO3-,Na+,Cl- |
| D、Ba2+,Cl-,K+,CO32- |
25℃、101kPa下,1mol氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O(1)△H=-285.8kJ/mol |
| B、2H2(g)+O2(g)=2H2O(1)△H=+571.6 kJ/mol |
| C、2H2(g)+O2(g)=2H2O(g)△H=-571.6 kJ/mol |
| D、H2(g)+O2(g)=H2O(1)△H=-285.8kJ/mol |